题目内容
12.下列有关气体摩尔体积的描述中正确的是( )| A. | 气体摩尔体积的数值是固定不变的,都约为22.4L | |
| B. | 通常情况的气体摩尔体积约为22.4L | |
| C. | 标准状况下的气体的摩尔体积约为22.4L | |
| D. | 标准状况下,气体的摩尔体积约为22.4L/mol |
分析 A.气体的摩尔体积由温度和压强决定;
B.通常状态为25度,101kKPa,1mol气体体积大于22.4L;
C.气体的摩尔体积单位为L/mol;
D.标况下,1mol任何气体体积大约22.4L.
解答 解:A.气体的摩尔体积由温度和压强共同决定的,温度、压强改变,气体摩尔体积就变,故A错误;
B.通常状态为25度,101kKPa,1mol气体体积大于22.4L,故错误;
C.标准状况下的气体的摩尔体积约为22.4L/mol,故C错误;
D.标准状况下,气体的摩尔体积约为22.4L/mol,故D正确;
故选:D.
点评 本题考查了气体摩尔体积,明确气体摩尔体积概念及单位是解题关键,注意标准状况下,气体的摩尔体积约为22.4L/mol,题目难度不大.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
20.核内中子数为N的R2+离子,质量数为A,则n克它的氧化物中所含质子的物质的量是( ) 摩尔.
| A. | $\frac{n(A-N+8)}{A+16}$ | B. | $\frac{n(A-N+10)}{(A+16)}$ | C. | A-N+2 | D. | $\frac{n(A-N+6)}{A}$ |
7.氯化亚铜常用作有机合成工业中的催化剂,为白色晶体,不溶于乙醇,微溶于水,易溶于浓盐酸形成络合离子[CuCl2]-.受潮露置空气中迅速氧化成碱式盐.实验室用下列流程制备:
注:①实验药品:硫酸铜晶体12.5g、氯化钠晶体6.0g、水200ml、铜粉3.5g、浓盐酸10ml.
②Na[CuCl2](易电离,溶液无色)$\frac{\underline{\;水\;}}{\;}$NaCl+CuCl↓ (白色沉淀).
请回答:
(1)写出实验室制取Na[CuCl2]的离子方程式Cu2++4Cl-+Cu=2[CuCl2]-.
(2)判断步骤②反应完全的现象是反应溶液由蓝色转变成无色透明时为止.
(3)步骤④有关抽滤操作,下列说法正确的是AD.
A.选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀
B.在吸滤瓶和抽气泵之间应连接一个安全瓶,吸滤瓶应与安全瓶的长导管相接
C.抽滤时不宜过滤胶状沉淀,否则易在滤纸上形成一层密实的沉淀
D.洗涤沉淀时,应关小水龙头,使洗涤剂缓缓通过沉淀物
(4)步骤⑤用乙醇的水溶液洗涤的目的是水洗涤除去氯化亚铜表面吸附的杂质,提高产品纯度,同时减少产品的溶解,减少损失.
(5)步骤⑥烘干须在真空干燥箱中进行,其原因是氯化亚铜在潮湿的空气中能迅速氧化生成碱式盐而变质.
(6)氯化亚铜的定量分析:
①取样品0.25g和10ml过量的FeCl3溶液于250ml锥形瓶中,充分溶解.
②用0.10mol•L-1硫酸锶铈标准溶液滴定.
已知:CuCl+FeCl3=CuCl2+FeCl2; Fe2++Ce4+=Fe3++Ce3+三次平行试验结果如下(平行试验结果相差不能超过1%):
则样品中CuCl的纯度为95.5%.(结果保留三位有效数字)

注:①实验药品:硫酸铜晶体12.5g、氯化钠晶体6.0g、水200ml、铜粉3.5g、浓盐酸10ml.
②Na[CuCl2](易电离,溶液无色)$\frac{\underline{\;水\;}}{\;}$NaCl+CuCl↓ (白色沉淀).
请回答:
(1)写出实验室制取Na[CuCl2]的离子方程式Cu2++4Cl-+Cu=2[CuCl2]-.
(2)判断步骤②反应完全的现象是反应溶液由蓝色转变成无色透明时为止.
(3)步骤④有关抽滤操作,下列说法正确的是AD.
A.选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀
B.在吸滤瓶和抽气泵之间应连接一个安全瓶,吸滤瓶应与安全瓶的长导管相接
C.抽滤时不宜过滤胶状沉淀,否则易在滤纸上形成一层密实的沉淀
D.洗涤沉淀时,应关小水龙头,使洗涤剂缓缓通过沉淀物
(4)步骤⑤用乙醇的水溶液洗涤的目的是水洗涤除去氯化亚铜表面吸附的杂质,提高产品纯度,同时减少产品的溶解,减少损失.
(5)步骤⑥烘干须在真空干燥箱中进行,其原因是氯化亚铜在潮湿的空气中能迅速氧化生成碱式盐而变质.
(6)氯化亚铜的定量分析:
①取样品0.25g和10ml过量的FeCl3溶液于250ml锥形瓶中,充分溶解.
②用0.10mol•L-1硫酸锶铈标准溶液滴定.
已知:CuCl+FeCl3=CuCl2+FeCl2; Fe2++Ce4+=Fe3++Ce3+三次平行试验结果如下(平行试验结果相差不能超过1%):
| 平行试验次数 | 1 | 2 | 3 |
| 0.25g样品消耗硫酸铈标准溶液的体积(ml) | 24.35 | 24.05 | 23.95 |
17.下面均是正丁烷与氧气反应的热化学方程式(25℃,101kPa):
①C4H10(g)+$\frac{13}{2}$O2 (g)═4CO2(g)+5H2O(l);△H=-2878KJ/mol
②C4H10(g)+$\frac{13}{2}$O2 (g)═4CO2(g)+5H2O(g);△H=-2658KJ/mol
③C4H10(g)+$\frac{9}{2}$O2 (g)═4CO(g)+5H2O(l);△H=-1746KJ/mol
④C4H10(g)+$\frac{9}{2}$O2 (g)═4CO(g)+5H2O(g);△H=-1526KJ/mol
由此判断,正丁烷的燃烧热是( )
①C4H10(g)+$\frac{13}{2}$O2 (g)═4CO2(g)+5H2O(l);△H=-2878KJ/mol
②C4H10(g)+$\frac{13}{2}$O2 (g)═4CO2(g)+5H2O(g);△H=-2658KJ/mol
③C4H10(g)+$\frac{9}{2}$O2 (g)═4CO(g)+5H2O(l);△H=-1746KJ/mol
④C4H10(g)+$\frac{9}{2}$O2 (g)═4CO(g)+5H2O(g);△H=-1526KJ/mol
由此判断,正丁烷的燃烧热是( )
| A. | 2878KJ/mol | B. | 2658KJ/mol | C. | 1746KJ/mol | D. | 1526KJ/mol |
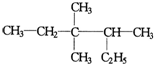 3,3,4-三甲基己烷
3,3,4-三甲基己烷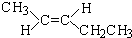 反-2-戊烯
反-2-戊烯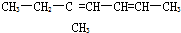 5-甲基-2,4一庚二烯
5-甲基-2,4一庚二烯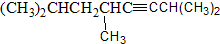 2,5,7-三甲基-3-辛炔.
2,5,7-三甲基-3-辛炔. “白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一.镀锌层犹如铁皮的保护层,这层膜的厚度及均匀度也成了判断镀层质量的重要指标.某研究性学习小组为了测定镀锌铁皮的厚度,设计了下面的实验方案:
“白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一.镀锌层犹如铁皮的保护层,这层膜的厚度及均匀度也成了判断镀层质量的重要指标.某研究性学习小组为了测定镀锌铁皮的厚度,设计了下面的实验方案: