题目内容
在2L容积不变的容器中,发生N2+3H2

2NH3的反应.现通入4mol H2和4mol N2,10s内用H2表示的反应速率为0.12mol/(L?s),则10s后容器中N2的物质的量是( )

2NH3的反应.现通入4mol H2和4mol N2,10s内用H2表示的反应速率为0.12mol/(L?s),则10s后容器中N2的物质的量是( )
| A.1.6mol | B.2.8mol | C.3.2mol | D.3.6mol |
v(H2)=0.12mol/(L?s),速率之比等于化学计量数之比,
所以v(N2)=
v(H2)=
×0.12mol/(L?s)=0.04mol/(L?s).
所以参加反应N2的物质的量为0.04mol/(L?s)×10s×2L=0.8mol.
所以10s后容器中N2的物质的量为4mol-0.8mol=3.2mol.
故选:C.
所以v(N2)=
| 1 |
| 3 |
| 1 |
| 3 |
所以参加反应N2的物质的量为0.04mol/(L?s)×10s×2L=0.8mol.
所以10s后容器中N2的物质的量为4mol-0.8mol=3.2mol.
故选:C.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
 2NH3的反应.现通入4mol H2和4mol N2,10s内用H2表示的反应速率为0.12mol/,则10s后容器中N2的物质的量是( )
2NH3的反应.现通入4mol H2和4mol N2,10s内用H2表示的反应速率为0.12mol/,则10s后容器中N2的物质的量是( )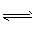 2NH3的反应。现通入4 molH2和4molN2,10 s内用H2表示的反应速率为0.12 mol/(L·s),则10 s后容器中N2的物质的量是
2NH3的反应。现通入4 molH2和4molN2,10 s内用H2表示的反应速率为0.12 mol/(L·s),则10 s后容器中N2的物质的量是