题目内容
下列选项中正确的是( )
| A、1L 0.5mol?L-1稀硫酸与1L 1mol?L-1氢氧化钠溶液反应放出57.3kJ的热量:H2SO4(aq)+2NaOH(aq)═Na2SO4(aq)+2H2O(l);△H=-57.3kJ?mol-1 | ||||
| B、某酸的酸式盐NaHY水溶液显碱性,则H2Y?2H++Y2- | ||||
| C、纯碱溶液显碱性的原因用离子方程式可表示为:CO32-+2H2O?H2CO3+2OH- | ||||
D、以惰性电极电解KCl溶液的离子方程式为:2Cl-+2H2O
|
考点:反应热和焓变,盐类水解的原理,盐类水解的应用,电解原理
专题:基本概念与基本理论
分析:A、酸碱反应中和热概念是强酸强碱的稀溶液反应生成1molH2O放出的热量;
B、某酸的酸式盐NaHY水溶液显碱性说明HY-是弱酸阴离子,水解大于电离程度;
C、纯碱溶液显碱性是因为碳酸根离子分步水解;
D、以惰性电极电解KCl溶液,生成氢氧化钾、氯气和水,结合离子方程式书写方法分析判断.
B、某酸的酸式盐NaHY水溶液显碱性说明HY-是弱酸阴离子,水解大于电离程度;
C、纯碱溶液显碱性是因为碳酸根离子分步水解;
D、以惰性电极电解KCl溶液,生成氢氧化钾、氯气和水,结合离子方程式书写方法分析判断.
解答:
解:A、酸碱反应中和热概念是强酸强碱的稀溶液反应生成1molH2O放出的热量,1L 0.5mol?L-1稀硫酸与1L 1mol?L-1氢氧化钠溶液反应放出57.3kJ的热量:H2SO4(aq)+2NaOH(aq)═Na2SO4(aq)+2H2O(l);△H=-114.6kJ?mol-1,故A错误;
B、某酸的酸式盐NaHY水溶液显碱性说明HY-是弱酸阴离子,水解大于电离程度,某酸的酸式盐NaHY水溶液显碱性,则H2Y?H++Y-,故B错误;
C、纯碱溶液显碱性是因为碳酸根离子分步水解,CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-,故C错误;
D、以惰性电极电解KCl溶液,生成氢氧化钾、氯气和水,电解的离子方程式为:2Cl-+2H2O
H2↑+2OH-+Cl2↑,故D正确;
故选D.
B、某酸的酸式盐NaHY水溶液显碱性说明HY-是弱酸阴离子,水解大于电离程度,某酸的酸式盐NaHY水溶液显碱性,则H2Y?H++Y-,故B错误;
C、纯碱溶液显碱性是因为碳酸根离子分步水解,CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-,故C错误;
D、以惰性电极电解KCl溶液,生成氢氧化钾、氯气和水,电解的离子方程式为:2Cl-+2H2O
| ||
故选D.
点评:本题考查了中和热概念分析,盐类水解的分析应用,电解原理分析判断,掌握基础是关键,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
用下列方法制取氢气,反应速率最大的是( )
| A、10℃时,粉末状锌与2mol?L-1硫酸溶液反应 |
| B、30℃时,粉末状锌与2mol?L-1硫酸溶液反应 |
| C、10℃时,块状锌与2mol?L-1硫酸溶液反应 |
| D、30℃时,块状锌与2mol?L-1硫酸溶液反应 |
已知:C(s)+H2O(I)=CO(g)+H2(g)△H1═+175.3kJ/mol
CO(g)+
O2(g)═CO2(g)△H2═-283.0kJ/mol
H2(g)+
O2(g)═H2O(Ⅰ)△H3═-283.0kJ/mol
则C(s)+O2(g)═CO2(g)的△H等于( )
CO(g)+
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
则C(s)+O2(g)═CO2(g)的△H等于( )
| A、390.7kj/mol |
| B、-679.3kj/mol |
| C、-787kj/mol |
| D、+180.9kj/mol |
油酸的结构简式为CH3(CH2)7CH=CH(CH2)7COOH,下列说法正确的是( )
| A、油酸的分子式为C18H33O2 |
| B、油酸是乙酸的同系物 |
| C、油酸可与氢气发生加成反应 |
| D、1mol油酸最多可与1mol甘油酯化 |
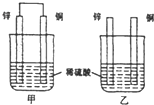 原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献.
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献.
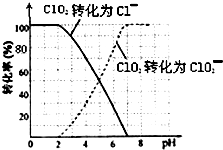 二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂.比Cl2更好.
二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂.比Cl2更好.