题目内容
1.工业上可利用CO2和H2生成甲醇,热化学方程式如下:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=Q1kJ•mol-1
又查资料得知:①CH3OH(l)+$\frac{1}{2}$O2(g)?CO2(g)+H2(g)△H=Q2kJ•mol-1
②H2O(g)=H2O(I)△H=Q3kJ•mol-1
则表示甲醇的燃烧热的热化学方程式为CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=(2Q1+3Q2+2Q3)kJ•mol-1.
分析 ①CO2(g)+3H2(g)?CH3OH(l)+H2O (g)△H=Q1kJ•mol-1
②CH3OH(l)+$\frac{1}{2}$O2(g)?CO2(g)+2H2(g)△H=Q2kJ•mol-1
③H2O(g)=H2O(l)△H=Q3kJ•mol-1,依据盖斯定律①×2+②×3+③×2计算得到.
解答 解:①CO2(g)+3H2(g)?CH3OH(l)+H2O (g)△H=Q1kJ•mol-1
②CH3OH(l)+$\frac{1}{2}$O2(g)?CO2(g)+2H2(g)△H=Q2kJ•mol-1
③H2O(g)=H2O(l)△H=Q3kJ•mol-1,依据盖斯定律①×2+②×3+③×2得到:
表示甲醇的燃烧热的热化学方程式为:CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=(2Q1+3Q2+2Q3) kJ•mol-1,
故答案为:CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=(2Q1+3Q2+2Q3) kJ•mol-1.
点评 本题考查盖斯定律,题目难度中等,明确反应过程是解题的关键,计算题简化计算过程,注意在学习中归纳总结.

练习册系列答案
相关题目
12.恒容密闭容器中发生如下反应:2NH3(g)+NO2(g)?2N2(g)+3H2O(g)△H<0,下列有关说法正确的是( )
| A. | 上述热化学方程式说明反应物的总键能大于生成物的总键能 | |
| B. | 达平衡后再通入NH3,则平衡正向移动,NH3转化率减小 | |
| C. | 达平衡后升温,则逆反应速率加快,正反应速率减慢,平衡逆向移动 | |
| D. | 达平衡后加入催化剂能同时增大正逆反应速率,平衡发生移动 |
9.应用元素周期律分析,下列推断正确的是( )
| A. | 砹(At)是第VIIA族元素,其氢化物的穆定性大于HCl | |
| B. | 铊(Tl)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应 | |
| C. | 第2周期非金属元素的气态氢化物溶于水后,水溶液均为酸性 | |
| D. | 第3周期金属元素最高价氧化物对应的水化物,其碱性随原子序数的增大而减弱 |
16.下列叙述Ⅰ和Ⅱ均正确并有因果关系的是( )
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 同主族元素的最外层电子数相同 | 同主族元素的化学性质一定相似 |
| B | 原电池可将化学能转化为电能 | 原电池需外接电源才能工作 |
| C | S的非金属性比Si强 | 酸性:H2SO4>H4SiO4 |
| D | Na在Cl2中燃烧的生成物含离子键 | NaCl固体可导电 |
| A. | A | B. | B | C. | C | D. | D |
6.广义的水解观认为:水解的物质和水分别离解成两部分,然后两两重新结合成新的物质,不出现元素化合价的变化.根据以上信息,下列物质水解后的产物错误的是( )
| A. | BaO2的水解产物是Ba(OH)2和H2O2 | B. | PCl3水解的产物是HClO和PH3 | ||
| C. | CaC2水解的产物是Ca(OH)2和C2H2 | D. | Al2S3水解的产物是Al(OH)3和H2S |
10.下列叙述正确的是( )
| A. | 向蒸馏水中滴加浓硫酸的过程中,Kw保持不变 | |
| B. | 酸与碱溶液恰好完全反应时所得溶液一定呈中性 | |
| C. | 向醋酸钠溶液中加入少量冰醋酸,水的电离度减小 | |
| D. | 广泛pH试纸能够测出溶液的精确pH |
 有机物A的结构简式为
有机物A的结构简式为 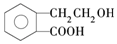 ,它可通过不同化学反应分别制得B、C、D和E四种物质.
,它可通过不同化学反应分别制得B、C、D和E四种物质.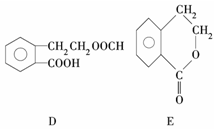
 .
. .
. +2NaOH→
+2NaOH→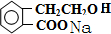 +HCOONa+H2O.
+HCOONa+H2O.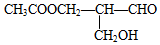 有光学活性,发生下列反应:
有光学活性,发生下列反应: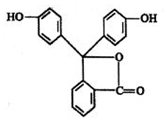 酚酞是白色结晶,在空气中稳定,几乎不溶于水,常用做酸碱指示剂,其结构简式如图:
酚酞是白色结晶,在空气中稳定,几乎不溶于水,常用做酸碱指示剂,其结构简式如图: