题目内容
5.在容积为2L的密闭容器中进行如下反应:A(g)+2B(g)?3C(g)+nD(g),开始时A为4mol,B为6mol;5min末时测得C的物质的量为6mol,用D表示的化学反应速率v(D)为0.4mol/(L•min).请回答下列有关问题:(1)5min末A的物质的量浓度为1mol/L.
(2)前5min内用B表示的化学反应速率v(B)为0.4mol/(L•min).
(3)化学方程式中n值为2.
(4)此反应在四种不同情况下的反应速率分别为:
①v(A )=5mol/( L•min ) ②v( B )=6mol/( L•min )
③v(C)=4.5mol/( L•min ) ④v(D )=8mol/( L•min )
其中反应速率最快的是①(填编号).
分析 5min末时测得C的物质的量为6mol,v(C)=$\frac{\frac{6mol}{2L}}{5min}$=0.6mol/(L•min),用D表示的化学反应速率v(D)为0.4mol/(L•min),由速率之比等于化学计量数之比可知,$\frac{0.6}{0.4}=\frac{3}{n}$,解得x=2,则
A(g)+2B(g)?3C(g)+2D(g)
开始 4 6 0 0
转化 2 4 6 4
平衡 2 2 6 4
结合v=$\frac{△c}{△t}$、c=$\frac{n}{V}$及反应速率与化学计量数的比值越大,反应速率越快来解答.
解答 解:5min末时测得C的物质的量为6mol,v(C)=$\frac{\frac{6mol}{2L}}{5min}$=0.6mol/(L•min),用D表示的化学反应速率v(D)为0.4mol/(L•min),由速率之比等于化学计量数之比可知,$\frac{0.6}{0.4}=\frac{3}{n}$,解得x=2,则
A(g)+2B(g)?3C(g)+2D(g)
开始 4 6 0 0
转化 2 4 6 4
平衡 2 2 6 4
(1)5min末A的物质的量浓度为$\frac{2mol}{2L}$=1mo1/L,故答案为:1mol/L;
(2)前5min内用B表示的化学反应速率v(B)为$\frac{\frac{4mol}{2L}}{5min}$=0.4mol/( L•min ),故答案为:0.4mol/( L•min );
(3)由上述分析可知,n=2,故答案为:2;
(4)反应速率与化学计量数的比值越大,反应速率越快,则①中$\frac{5}{1}$=5,②中$\frac{6}{2}$=3,③中$\frac{4.5}{3}$=1.5,④中$\frac{8}{2}$=4,显然①中比值最大,反应速率最快,
故答案为:①.
点评 本题考查化学平衡的计算,为高频考点,把握平衡三段法、速率的计算及比较反应快慢为解答的关键,侧重分析与计算能力的考查,注意n的确定方法,题目难度不大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 停止冬季供暖,减少有害物质排放 | |
| B. | 对锅炉和汽车等产生的有害气体和烟尘进行处理 | |
| C. | 退耕还林,改善生态环境 | |
| D. | 寻找新能源,减少化石燃料的使用 |
| A. | 分子式为C5H11CI的有机物,分子结构中含2个甲基的同分异构体有4种 | |
| B. | CH3COOH与C2H518OH在浓硫酸作用下加热,反应生有机物分子的结构简式为CH3COOC2H5 | |
| C. | 三氯甲烷只有一种结构,不存在同分异构,证明甲烷是正四面体构型 | |
| D. | 煎炸食物的花生油和牛油都是可皂化的饱和醋类 |
| A. | K+ 1s22s22p63s23p6 | B. | F 1s22s22p5 | ||
| C. | S2- 1s22s22p63s23p4 | D. | Ar 1s22s22p63s23p6 |
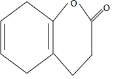 的同分构体中只有一个支链且能与NaHCO3溶液反应的芳香族化合物有(不考虑立体异构)( )
的同分构体中只有一个支链且能与NaHCO3溶液反应的芳香族化合物有(不考虑立体异构)( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
| A. | 4mol | B. | 8mol | C. | 10mol | D. | 2mol |
 太阳能电池的发展已经进入了第三代.第三代就是铜铟镓硒CIGS等化合物薄膜太阳能电池以及薄膜硅系太阳能电池.完成下列填空:
太阳能电池的发展已经进入了第三代.第三代就是铜铟镓硒CIGS等化合物薄膜太阳能电池以及薄膜硅系太阳能电池.完成下列填空: