题目内容
某化学反应2A![]() B+D在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
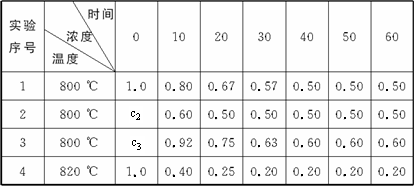
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为________mol·(L·min)-1.
(2)在实验2,A的初始浓度c2=________mol·L-1,反应经20分钟就达到平衡,可推测实验2中还隐含的反应条件是________.
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3________v1(填“>”“=”或“<”)且c3________1.0 mol·L-1(填“>”“=”或“<”)
(4)比较实验4和实验1,可推测反应速率快的是________,理由是________
________.
解析:
|
思路解析:本题综合考查了浓度、温度、催化剂对化学反应速率的影响.此题综合性较强,要综合考虑浓度、温度、催化剂对化学反应速率的影响,从而对影响反应速率的时间变化表格,提出合理的解释并定量计算.不同的实验条件或同一次实验的不同时刻,浓度的变化是不同的,故在Δt时间内的浓度变化应视为这段时间内的平均速率.实验1,在反应后10至20分钟内的平均速率应为v(A)= 实验2,在相同反应温度下,达到平衡时A的浓度不变,但达到平衡的时间缩短了,故推测A的初始浓度并没有变,即c2=1 mol·L-1,但反应中使用了催化剂.实验3,在相同反应温度下,达到平衡时A的浓度变大了,且在相同的时间间隔10至20分钟内,A的浓度变化量增至0.92 mol-0.75 mol=0.17 mol,故可推测v3>v1,且c3>1.0 mol·L-1.实验4,温度高,速率快. 绿色通道:本题给出了在不同条件下进行的四次实验数据,要求通过对反应物A的浓度在1小时的各个时间间隔内浓度变化数值共计32个数据的分析、判断,推出各次实验中起始浓度增大还是减小,反应速率是快还是慢,什么时候达到平衡,哪次实验中使用了催化剂……本题要求掌握数据的分析、判断、比较、推理的方法.特别注意计算理解表格中差量的变化趋势和含义.这种以能力立意并将研究性学习方法渗透到基础性学习内容中去的构思值得注意. 反应速率的快慢、平衡的判断、催化剂的作用可以通过文字,还可通过图象和表格表达出来.根据图象和表格可以更加直观、深刻地理解速率、平衡. |

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案某化学反应2A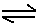 B+D在四种不同条件下进行。B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行。B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
|
实验序号 |
|
0 |
10 |
20 |
30 |
40 |
50 |
60 |
|
1 |
800℃ |
1.0 |
0.80 |
0.67 |
0.57 |
0.50 |
0.50 |
0.50 |
|
2 |
800℃ |
c2 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
|
3 |
800℃ |
c3 |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
|
4 |
820℃ |
1.0 |
0.40 |
0.25 |
0.20 |
0.20 |
0.20 |
0.20 |
根据上述数据,完成下列填空:
(1)在实验1中,反应在10至20分钟内平均速率为 。
(2)在实验2中,A的初始浓度c2=______ ____,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是______ ____。
(3)设实验3中的反应速率为v3,实验1的反应速率为v1,则v3__________v1(填“>”、“=”或“<”),且c3__________1.0mol·L-1(填“<”、“=”或“>”)。
(4)比较实验4和实验1,可推测该反应是__________反应(填“吸热”或“放热”)。
 B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表: B+D在三种不同条件下进行,B、D的起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B+D在三种不同条件下进行,B、D的起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表: