题目内容
发射“神舟”系列飞船的长征火箭用肼(N2H4)作为燃料,N2H4与NH3有相似的化学性质.
(1)写出肼的电子式 ;
(2)用拉席希法制备肼,是将NaClO和NH3反应生成肼,试写出该反应的化学方程式 .
(3)在锅炉水中加入N2H4,可以把锅炉表面的氧化铁还原为结构紧密的四氧化三铁保护层,写出N2H4被氧化的化学反应方程式 .
(4)通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.
发射火箭时肼(N2H4)为液态燃料,若在O2(气态)中燃烧,生成N2(气态)和H2O(液态).写出肼燃烧的热化学方程式 .
(5)发射火箭时肼(N2H4)为燃料,也可以二氧化氮或氟气作氧化剂,分别写出化学方程式: 、 .
(6)对比O2、F2、H2O2、NO2四种助燃剂,放出热量最多时应选用 ;实际我们选用的助燃剂是NO2,主要考虑的因素是 .
(1)写出肼的电子式
(2)用拉席希法制备肼,是将NaClO和NH3反应生成肼,试写出该反应的化学方程式
(3)在锅炉水中加入N2H4,可以把锅炉表面的氧化铁还原为结构紧密的四氧化三铁保护层,写出N2H4被氧化的化学反应方程式
(4)通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.
| 化学键 | N-H | N-N | O=O | N≡N | O-H |
| 键能/KJ?mol-1 | 386 | 167 | 498 | 946 | 460 |
(5)发射火箭时肼(N2H4)为燃料,也可以二氧化氮或氟气作氧化剂,分别写出化学方程式:
(6)对比O2、F2、H2O2、NO2四种助燃剂,放出热量最多时应选用
考点:电子式,热化学方程式,氨的化学性质
专题:化学反应中的能量变化,元素及其化合物
分析:(1)氨分子中氢原子被氨基(-NH2)取代后的生成物叫肼,分子中全部为单键;
(2)NaClO和NH3按物质的量之比为1:2,则NH3和NaClO的计量数2:1,然后根据原子守恒分析;
(3)在锅炉水中加入N2H4,可以把锅炉表面的氧化铁还原为结构紧密的四氧化三铁保护层,N2H4 被氧化,且反应中无污染物生成,N2H4被氧化为氮气,同时生成水;
(4)先写出化学方程式,然后根据焓变=反应物的总键能-生成物的总键能计算焓变;
(5)肼和二氧化氮反应生成氮气和水;和氟气反应生成氮气和氟化氢;
(6)氟气放出的热量最多,但生成氟化氢有污染.
(2)NaClO和NH3按物质的量之比为1:2,则NH3和NaClO的计量数2:1,然后根据原子守恒分析;
(3)在锅炉水中加入N2H4,可以把锅炉表面的氧化铁还原为结构紧密的四氧化三铁保护层,N2H4 被氧化,且反应中无污染物生成,N2H4被氧化为氮气,同时生成水;
(4)先写出化学方程式,然后根据焓变=反应物的总键能-生成物的总键能计算焓变;
(5)肼和二氧化氮反应生成氮气和水;和氟气反应生成氮气和氟化氢;
(6)氟气放出的热量最多,但生成氟化氢有污染.
解答:
解:(1)氨分子中氢原子被氨基(-NH2)取代后的生成物叫肼,分子中全部为单键,电子式为: ,故答案为:
,故答案为: ;
;
(2)NaClO和NH3按物质的量之比为1:2,则NH3和NaClO的计量数2:1,结合原子守恒可知反应为2NH3+NaClO=N2H4+NaCl+H2O,故答案为:NaClO+2NH3═NaCl+N2H4+H2O;
(3)在锅炉水中加入N2H4,可以把锅炉表面的氧化铁还原为结构紧密的四氧化三铁保护层,N2H4 被氧化,且反应中无污染物生成,N2H4被氧化为氮气,同时生成水,反应的化学方程式为6Fe2O3+N2H4=4Fe3O4+N2↑+2H2O,故答案为:6Fe2O3+N2H4═N2+4Fe3O4+2H2O;
(4)N2H4燃烧的化学方程式为N2H4(g)+O2(g)═N2(g)+2H2O(g),△H=反应物的总键能-生成物的总键能=167 kJ?mol-1+386 kJ?mol-1×4+498 kJ?mol-1-946 kJ?mol-1-460 kJ?mol-1×4=-577 kJ?mol-1,所以N2H4燃烧的热化学方程式为N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-577 kJ?mol-1,故答案为:N2H4(l)+O2(g)═N2(g)+2H2O(l)△H=-577kJ/mol;
(5)肼和二氧化氮反应生成氮气和水,化学方程式2N2H4+2NO2═3N2+4H2O;和氟气反应生成氮气和氟化氢,化学方程式N2H4+2F2═N2+4HF,故答案为:2N2H4+2NO2═3N2+4H2O;N2H4+2F2═N2+4HF;
(6)氟气放出的热量最多,但生成氟化氢有污染;NO2易液化,产物为氮气和水,无污染,故答案为:F2;燃烧产物无污染,NO2易液化.
 ,故答案为:
,故答案为: ;
;(2)NaClO和NH3按物质的量之比为1:2,则NH3和NaClO的计量数2:1,结合原子守恒可知反应为2NH3+NaClO=N2H4+NaCl+H2O,故答案为:NaClO+2NH3═NaCl+N2H4+H2O;
(3)在锅炉水中加入N2H4,可以把锅炉表面的氧化铁还原为结构紧密的四氧化三铁保护层,N2H4 被氧化,且反应中无污染物生成,N2H4被氧化为氮气,同时生成水,反应的化学方程式为6Fe2O3+N2H4=4Fe3O4+N2↑+2H2O,故答案为:6Fe2O3+N2H4═N2+4Fe3O4+2H2O;
(4)N2H4燃烧的化学方程式为N2H4(g)+O2(g)═N2(g)+2H2O(g),△H=反应物的总键能-生成物的总键能=167 kJ?mol-1+386 kJ?mol-1×4+498 kJ?mol-1-946 kJ?mol-1-460 kJ?mol-1×4=-577 kJ?mol-1,所以N2H4燃烧的热化学方程式为N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-577 kJ?mol-1,故答案为:N2H4(l)+O2(g)═N2(g)+2H2O(l)△H=-577kJ/mol;
(5)肼和二氧化氮反应生成氮气和水,化学方程式2N2H4+2NO2═3N2+4H2O;和氟气反应生成氮气和氟化氢,化学方程式N2H4+2F2═N2+4HF,故答案为:2N2H4+2NO2═3N2+4H2O;N2H4+2F2═N2+4HF;
(6)氟气放出的热量最多,但生成氟化氢有污染;NO2易液化,产物为氮气和水,无污染,故答案为:F2;燃烧产物无污染,NO2易液化.
点评:本题考查化学方程式的书写,反应热等,题目难度较大,反应物与产物的判断是解题的关键.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
下列有关反应限度的叙述正确的是( )
| A、平衡常数K的大小能说明反应的限度,因此当平衡右移时,K值必定增大 |
| B、可逆反应达到平衡状态后,改变外界条件后,若反应速率发生变化,则平衡一定发生移动 |
| C、若反应2A(g)+B(g)?2C(g)是自发反应,则该反应的△H<0 |
| D、使用催化剂可降低反应活化能,加快反应速率,改变反应限度 |
下列有关溶液的说法中,正确的是( )
| A、不饱和溶液转化为饱和溶液,溶液中溶质的质量分数一定增大 |
| B、将一定质量某物质的饱和溶液降温析出晶体后,所得溶液中溶质的质量一定减小 |
| C、饱和溶液不一定是浓溶液,不饱和溶液一定是稀溶液 |
| D、将5g某物质完全溶解于95g水中,所得溶液中溶质的质量分数一定是5% |
下列电子式中,错误的是( )
| A、Na+ |
B、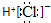 |
C、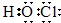 |
D、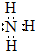 |
下列各组物质在一定条件下发生的反应不属于中和反应的是( )
| A、NH3+H2O |
| B、H2+CuO |
| C、NaHCO3+HCl |
| D、(NH4)2S+NaOH→NH3↑ |