题目内容
(10分)某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
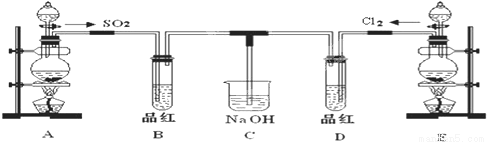
(1)实验室用装置A制备SO2.某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能: ;
(2)实验室用装置E制备Cl2,其反应的化学方程式为:MnO2+4HCl(浓)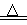 MnCl2+Cl2↑+2H2O。若有0.6 mol的HCl参加反应,则转移的电子总数为 mol;
MnCl2+Cl2↑+2H2O。若有0.6 mol的HCl参加反应,则转移的电子总数为 mol;
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:
B: ,D: ;
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象是:
B: ,D: ;
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强.他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样.请你分析该现象的原因(用化学方程式表示): 。如果用0.01 mol SO2与0.01 mol Cl2同时非常缓慢地通入100 mL水中,假如得到的溶液体积仍为100 mL,则所得溶液中氢离子的物质的量浓度约为 。
(共10分,每小题2分)(1)分液漏斗的玻璃塞没有取下来 (2)0.3
(3)①品红褪色,品红褪色 ②褪色的品红又恢复成红色,无明显现象
(4)Cl2+SO2+2H2O=2HCl+H2SO4 0.4 mol.L-1(单位不写或写错都不给分)
【解析】
试题分析:(1)塞子没有取下来,打开活塞时,空气无法进入分液漏斗内部,造成分液漏斗内的压强小于大气压强,液体无法流出,故答案为:分液漏斗的玻璃塞没有取下来;
(2)在反应MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O中,每有4mol HCl参与反应,被氧化的氯化氢是2mol,即被氧化的氯化氢占参与反应的50%,0.6 molHCl参加反应被氧化的氯化氢是0.3mol,转移的电子数为0.3NA,故答案为:0.3NA;
MnCl2+Cl2↑+2H2O中,每有4mol HCl参与反应,被氧化的氯化氢是2mol,即被氧化的氯化氢占参与反应的50%,0.6 molHCl参加反应被氧化的氯化氢是0.3mol,转移的电子数为0.3NA,故答案为:0.3NA;
(3)SO2具有漂白性,二氧化硫通入品红溶液中,品红褪色;SO2的漂白具有可逆性,褪色后的溶液加热时又恢复原来的红色。氯气和水反应生成的次氯酸具有漂白性,因而氯气通入品红溶液中也能使品红褪色,次氯酸的漂白不可逆,加热时,不能恢复红色,故答案为:品红褪色;品红褪色;褪色的品红又恢复成红色;无明显现象;
(4)氯气具有较强的氧化性,二氧化硫具有较强的还原性,在水溶液中两者1:1发生反应:Cl2+SO2+2H2O=2HCl+H2SO4,生成物都无漂白性,因而SO2和Cl2按1:1同时通入到品红溶液时,品红溶液并不退色;如果用0.01 mol SO2与0.01 mol Cl2同时非常缓慢地通入100 mL水中,则根据方程式可知生成盐酸和硫酸的物质的量分别是0.02mol和0.01mol,其中氢离子的物质的量是0.04mol,则假如得到的溶液体积仍为100 mL,因此所得溶液中氢离子的物质的量浓度约为0.04mol÷0.1L=0.4mol/L,故答案为:Cl2+SO2+2H2O═4H++2Cl-+SO42-;0.4mol/L。
考点:考查氯气和二氧化硫的漂白性质实验设计与探究

(13分)根据要求完成下列各小题实验目的。(a、b 为弹簧夹,加热及固定装置已略去)
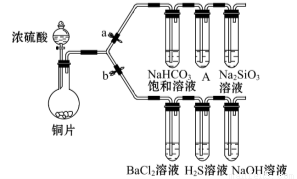
(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸 >碳酸)
①连接仪器、 、加药品后,打开a关闭 b,然后滴入浓硫酸,加热。
②铜与浓硫酸反应的化学方程式是__________________,装置A中的试剂是 。
③能说明碳的非金属性比硅强的实验现象是:_______________________。
(2)验证 SO2的氧化性、还原性和酸性氧化物的通性。
①打开b,关闭a。能验证SO2具有氧化性的化学方程式是:___________。
②若大量的SO2通入NaOH溶液中,其化学方程式是:__________________。
③BaCl2溶液中无沉淀现象,将其分成两份,分別滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
滴加的溶液 | 氯 水 | 氨 水 |
沉淀的化学式 |
|
|
写出其中SO2 显示还原性并生成沉淀的离子方程式___________________。
 、SO
、SO 、CO
、CO 、NO
、NO 。取200 mL该溶液,分为等体积的两份分别做下列实验。实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224 mL。实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33 g。下列说法正确的是( )
。取200 mL该溶液,分为等体积的两份分别做下列实验。实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224 mL。实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33 g。下列说法正确的是( )