题目内容
部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如下处理: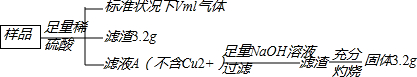
(1)样品中Fe元素的质量为 g;
(2)产生的气体的体积V= mL;
(3)溶液A中的阳离子有 .
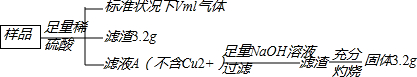
(1)样品中Fe元素的质量为
(2)产生的气体的体积V=
(3)溶液A中的阳离子有
考点:常见金属元素的单质及其化合物的综合应用,有关混合物反应的计算
专题:几种重要的金属及其化合物
分析:硫酸足量,由氧化性:Fe3+>Cu2+>H+,铁离子优先反应,由于滤液A中不含铜离子,且有气体氢气生成,则滤液A中不含铁离子,滤渣3.2g为金属铜,物质的量为0.05mol,即合金样品中总共含有铜元素0.05mol,滤液A中加入足量氢氧化钠溶液,所得滤渣灼烧得到的固体3.2g为Fe2O3,物质的量为0.02mol,铁元素的物质的量为0.04mol,以此来解答.
解答:
解:硫酸足量,由于氧化性:Fe3+>Cu2+>H+,铁离子优先反应,由于滤液A中不含铜离子,且有气体氢气生成,则滤液A中不含铁离子,滤渣3.2g为金属铜,物质的量为0.05mol,即合金样品中总共含有铜元素0.05mol,滤液A中加入足量氢氧化钠溶液,所得滤渣灼烧得到的固体3.2g为Fe2O3,
(1)Fe的物质的量为
×2=0.04mol,其质量为0.04mol×56g/mol=2.24g,故答案为:2.24;
(2)最后溶液中溶质为过量H2SO4和FeSO4,而铁元素物质的量为0.04mol,说明参加反应硫酸物质的量为0.04mol,含氢离子0.08mol,其中部分氢离子生成氢气,另外的H+和合金中的氧结合成水了,由于合金中氧物质的量
=0.02mol,它结合氢离子0.04mol,所以硫酸中有0.08-0.04=0.04molH+生成氢气,即生成0.02mol氢气,标况体积为448ml,故答案为:448;
(3)生成的滤渣3.2g是铜,金属铜可以和三价铁反应,所以一定不含有+3价铁离子,则溶液A中含Fe2+、H+,故答案为:Fe2+、H+.
(1)Fe的物质的量为
| 3.2g |
| 160g/mol |
(2)最后溶液中溶质为过量H2SO4和FeSO4,而铁元素物质的量为0.04mol,说明参加反应硫酸物质的量为0.04mol,含氢离子0.08mol,其中部分氢离子生成氢气,另外的H+和合金中的氧结合成水了,由于合金中氧物质的量
| 5.76g-3.2g-2.24g |
| 16g/mol |
(3)生成的滤渣3.2g是铜,金属铜可以和三价铁反应,所以一定不含有+3价铁离子,则溶液A中含Fe2+、H+,故答案为:Fe2+、H+.
点评:本题考查金属及化合物的性质、混合物分离提纯综合应用等,为高频考点,把握物质的性质及氧化还原反应等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
砷是氮族元素,黄砷(As4)是其一种单质,其分子结构与白磷(P4)相似,以下关于黄砷与白磷的比较叙述正确的是( )
| A、分子中共价键键角均为60° |
| B、黄砷中共价键键能大于白磷 |
| C、分子中含有的共价键的数目都是4 |
| D、黄砷的熔点低于白磷 |
提纯含有少量Ba(NO3)2杂质的KNO3溶液,可以使用的方法是( )
| A、加入过量的K2CO3溶液,过滤,除去沉淀,滤液中补加适量硝酸 |
| B、加入过量的K2SO4溶液,过滤,除去沉淀,滤液中补加适量硝酸 |
| C、加入过量的Na2CO3溶液,过滤,除去沉淀,滤液中补加适量硝酸 |
| D、加入过量的Na2SO4溶液,过滤,除去沉淀,滤液中补加适量硝酸 |
如图两种化合物的结构或性质描述正确的是( )
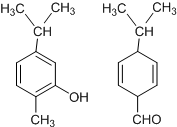

| A、不是同分异构体 |
| B、均是芳香族化合物 |
| C、均能与溴水反应 |
| D、可用红外光谱区分,但不能用核磁共振氢谱区分 |
将适量的Na2O2用脱脂棉包裹起来,然后用胶头滴管向脱脂棉(有利于水渗透)上滴上几滴水,很快脱脂棉就剧烈燃烧起来.由此实验现象无法得出的结论是( )
| A、反应过程中有热量放出 |
| B、反应过程中助燃剂O2生成 |
| C、反应过程中有NaOH生成 |
| D、脱脂棉发生了氧化反应 |
化学在生产和日常生活中有着重要的应用,下列说法不正确的是( )
| A、MgO和Al2O3都可以做耐高温材料 |
| B、Si可用作太阳能电池材料 |
| C、工业上采用电解水法制氢气,解决能源短缺 |
| D、氢氧化铝用于治疗胃酸过多 |
分子式为C7H8的某有机物,它能使酸性高锰酸钾溶液褪色,但不能与溴水反应.在一定条件下与H2完全加成,加成产物一氯代物的同分异构体数目与该有机物一氯代物的同分异构体数目相比( )
| A、前者多 | B、后者多 |
| C、一样多 | D、无法确定 |
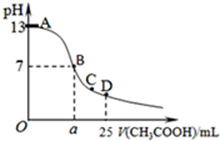 某温度时,在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图乙所示,有关粒子浓度关系的比较正确的是
某温度时,在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图乙所示,有关粒子浓度关系的比较正确的是( )
| A、在D点:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
| B、在C点:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| C、在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+) |
| D、在A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
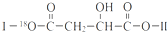 (其中Ⅰ、Ⅱ为未知部分的结构).下列是X发生反应的转化关系图及E的信息.
(其中Ⅰ、Ⅱ为未知部分的结构).下列是X发生反应的转化关系图及E的信息.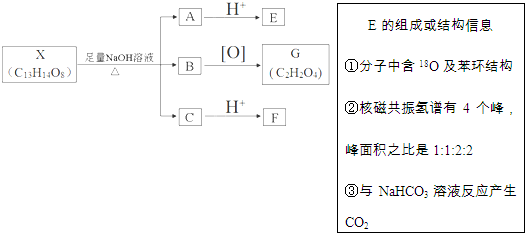
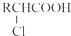 ,RCH2Br
,RCH2Br