题目内容
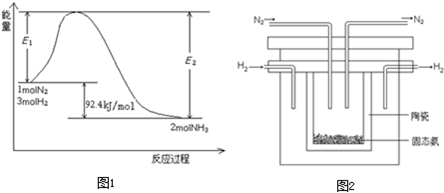
将33.9 g表面已被氧化的铝粉和过氧化钠的混合物放入一定量的水中,充分反应后固体无剩余。用密闭容器收集产生的气体,并用点火花引燃,气体恰好完全反应。再向混合液中加入750 mL 1 mol·L-1的硫酸,可使反应过程中产生的沉淀刚好消失。求:(1)原混合物中各物质的质量各多少克?
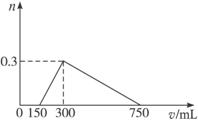
(2)画出向混合液中加入硫酸时,消耗硫酸的体积V(mL)与产生沉淀的物质的量n(mol)的关系图。
(1)m(Al)=5.4 g m(Al2O3)=5.1 g m(Na2O2)=23.4 g
(2)
解析:(1)混合物为Al、Al2O3、Na2O2,它们在水中发生的反应分别为:
2Na2O2+2H2O====4NaOH+O2↑,Al2O3+2NaOH====H2O+2NaAlO2,2Al+2NaOH+2H2O====2NaAlO2+3H2↑
密闭容器中进行的反应为:2H2+O2====2H2O,加入硫酸后又发生了反应2NaOH+H2SO4====Na2SO4+2H2O,2NaAlO2+H2SO4+2H2O====2Al(OH)3↓+Na2SO4,2Al(OH)3+3H2SO4====Al2(SO4)3+3H2O。可见,最后所得溶液中的溶质是Na2SO4、Al2(SO4)3。
设原混合物中含n(Al)=x,n(Al2O3)=y,n(Na2O2)=z,则综合考虑上述七个化学方程式和题给数据可建立以下方程式:27 g·mol-1×x+102 g·mol-1×y+78 g·mol-1×z=33.9 g(①式),1.5x=z(②式)1×0.750 mol·L-1=z+3(x+2y)/2(③式),联立①②③式并解之,x=0.2 mol,y=0.05 mol,z=0.3 mol。进而可知:m(Al)=5.4 g,m(Al2O3)=5.1 g,m(Na2O2)=23.4 g。

练习册系列答案
相关题目