题目内容
9.2A(g)?2B(g)+C(g);正反应吸热,达平衡时,要使v(正)增大、c(A)减小,应采取( )| A. | 加压 | B. | 减压 | C. | 减小B的浓度 | D. | 升温 |
分析 达平衡时,要使v正增大,可采取升高温度、增大压强或增加浓度的措施,使c(A)减少,应使平衡向正反应方向移动,由此分析解答.
解答 解:A、加压v(正)增大、,平衡逆向移动,c(A)增大,故A错误;
B、减压v(正)减小,故B错误;
C、减小B的浓度,导致v(正)减小,故C错误;
D、升温v正增大,平衡正向移动,所以c(A)减小,故D正确;
故选D.
点评 本题考查外界条件对化学平衡的影响,题目难度不大,本题注意根据反应方程式的特征判断平衡移动的方向.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.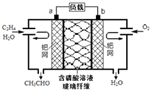 乙烯催化氧化成乙醛可设计成如图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应为:2CH2=CH2+O2→2CH3CHO.下列有关说法正确的是( )
乙烯催化氧化成乙醛可设计成如图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应为:2CH2=CH2+O2→2CH3CHO.下列有关说法正确的是( )
 乙烯催化氧化成乙醛可设计成如图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应为:2CH2=CH2+O2→2CH3CHO.下列有关说法正确的是( )
乙烯催化氧化成乙醛可设计成如图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应为:2CH2=CH2+O2→2CH3CHO.下列有关说法正确的是( )| A. | a电极发生还原反应 | |
| B. | 放电时,每转移2mol电子,理论上需要消耗28g乙烯 | |
| C. | b极反应式为:O2+4e-+2H2O═4OH- | |
| D. | 电子移动方向:电极a→磷酸溶液→电极b |
7.下列离子在溶液中能大量共存的是( )
| A. | Na+、CO32-、SO42-、H+ | B. | K+、AlO2-、H+、Cl- | ||
| C. | Fe3+、K+、OH-、NO3- | D. | Al3+、H+、NO3-、SO42- |
17.下列说法不正确的是( )
| A. | 在干旱地区植树造林时,可利用高吸水性树脂抗旱保水 | |
| B. | 硅酸钠的水溶液俗称水玻璃,是制备硅胶和木材防火剂的原料 | |
| C. | 在食用盐中加入碘单质制得的加碘盐.可用于预防大脖子病 | |
| D. | 服用阿司匹林若出现水杨酸反应,应立即停药并静脉滴注NaHCO3溶液 |
14.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 过氧化钠与水反应时,生成22.4L氧气转移的电子数为2 NA | |
| B. | 18g D2O中含有的电子数和中子数均为10 NA | |
| C. | 密闭容器中2mol NO与1mol O2充分反应,产物的分子数为2 NA | |
| D. | 1mol Na与足量的O2反应,生成Na2O和Na2O2的混合物,钠失去 NA个电子 |
1.下列说法正确的是( )
| A. | 在101kPa时,1molS完全燃烧生成SO3时所放出的热量,是S的燃烧热 | |
| B. | 吸热反应必须加热才能反应,放热反应不需要加热 | |
| C. | 在101kPa时,1mol S和2mol S的燃烧热相同 | |
| D. | 在稀溶液中,H2SO4和Ba(OH)2完全中和产生1mol水时放出的热量为57.3kJ |
18.丙酮是一种常用的有机溶剂,可与水以任意体积比互溶,沸点约55℃,分离水和丙酮时最合理的方法是( )
| A. | 蒸馏 | B. | 分液 | C. | 过滤 | D. | 蒸发 |
19.(1)为达下表所列实验目的,请选择合适的实验方法,将其标号填在相应的空格中.
A、加热至恒重 B、用氢氧化钠溶液溶解后过滤
C.溶解、过滤、结晶 D.滴加KSCN溶液观察是否溶液是否变红
(2)实验室有甲、乙两瓶无色溶液,其中一瓶是稀盐酸,另一瓶是碳酸钠溶液.为鉴别两溶液,进行以下实验:取甲溶液于试管,向其中缓慢滴入乙溶液,并边滴加边振荡,观察到开始无明显现象,后来有大量气体生成.甲是Na2CO3溶液;
实验过程中所发生反应的离子方程式为:CO32-+H+=HCO3-、HCO3-+H+=CO2+H2O;
(3)将CO2和SO2气体分别通入酸性高锰酸钾,使之褪色的是SO2气体,请写出该反应的离子方程式:5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+.
| 实验目的 | 标号 |
| 检验氯化亚铁是否变质 | |
| 除去食盐中少量细砂 | |
| 除去碳酸钠固体中少量碳酸氢钠 | |
| 除去镁粉中混有的少量铝粉 |
C.溶解、过滤、结晶 D.滴加KSCN溶液观察是否溶液是否变红
(2)实验室有甲、乙两瓶无色溶液,其中一瓶是稀盐酸,另一瓶是碳酸钠溶液.为鉴别两溶液,进行以下实验:取甲溶液于试管,向其中缓慢滴入乙溶液,并边滴加边振荡,观察到开始无明显现象,后来有大量气体生成.甲是Na2CO3溶液;
实验过程中所发生反应的离子方程式为:CO32-+H+=HCO3-、HCO3-+H+=CO2+H2O;
(3)将CO2和SO2气体分别通入酸性高锰酸钾,使之褪色的是SO2气体,请写出该反应的离子方程式:5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+.