题目内容
25℃时,将0.01molCH3COONa和0.002molHCl溶于水,形成1L混合溶液:
(1)该溶液中存在着三个平衡体系,用电离方程式或离子方程式表示:① ,② ,③ .
(2)溶液中共有 种粒子(指分子和离子)
(3)在这些粒子中,浓度是0.01mol?L-1的是 .
(1)该溶液中存在着三个平衡体系,用电离方程式或离子方程式表示:①
(2)溶液中共有
(3)在这些粒子中,浓度是0.01mol?L-1的是
考点:盐类水解的应用,弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:(1)该溶液中存在弱电解质水和醋酸的电离、醋酸根离子盐类水解;
(2)0.01molCH3COONa和0.002molHCl溶于水得到0.008molCH3COONa、0.002molCH3COOH、0.002molNaCl,CH3COONa、NaCl为强电解质,CH3COOH为弱电解质,据此进行解答;
(3)醋酸钠的物质的量为0.01mol,物质的量浓度为0.01mol/L,钠离子浓度为0.01mol/L.
(2)0.01molCH3COONa和0.002molHCl溶于水得到0.008molCH3COONa、0.002molCH3COOH、0.002molNaCl,CH3COONa、NaCl为强电解质,CH3COOH为弱电解质,据此进行解答;
(3)醋酸钠的物质的量为0.01mol,物质的量浓度为0.01mol/L,钠离子浓度为0.01mol/L.
解答:
解:(1)存在水的电离平衡、醋酸的电离平衡、醋酸根离子的水解平衡,分别为H2O?H++OH-、CH3COOH?CH3COO-+H+、CH3COO-+H2O?CH3COOH+OH-,
故答案为:H2O?H++OH-;CH3COOH?CH3COO-+H+;CH3COO-+H2O?CH3COOH+OH-;
(2)0.01molCH3COONa和0.002molHCl溶于水得到0.008molCH3COONa、0.002molCH3COOH、0.002molNaCl,CH3COONa、NaCl为强电解质,CH3COOH为弱电解质,则溶液中存在的离子为:Na+、H+、Cl-、OH-、CH3COO-,存在的分子为:H2O、CH3COOH,即共有7种不同的微粒,
故答案为:7;
(3)CH3COONa的物质的量为0.01mol,醋酸钠的物质的量浓度为0.01mol/L,则浓度为0.01mol?L-1的是Na+,故答案为:Na+.
故答案为:H2O?H++OH-;CH3COOH?CH3COO-+H+;CH3COO-+H2O?CH3COOH+OH-;
(2)0.01molCH3COONa和0.002molHCl溶于水得到0.008molCH3COONa、0.002molCH3COOH、0.002molNaCl,CH3COONa、NaCl为强电解质,CH3COOH为弱电解质,则溶液中存在的离子为:Na+、H+、Cl-、OH-、CH3COO-,存在的分子为:H2O、CH3COOH,即共有7种不同的微粒,
故答案为:7;
(3)CH3COONa的物质的量为0.01mol,醋酸钠的物质的量浓度为0.01mol/L,则浓度为0.01mol?L-1的是Na+,故答案为:Na+.
点评:本题考查溶液中的微粒及电离方程式、水解方程式的书写,题目难度不大,明确混合溶液中的溶质、电解质的强弱、原子守恒等知识是解答本题的关键.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目

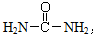 ,请写出尿素的同分异构体中含有离子键的化学式
,请写出尿素的同分异构体中含有离子键的化学式