题目内容
已知:
①硫酸比次氯酸稳定;
②高氯酸是比硫酸更强的酸;
③S2-易被氯气氧化;
④氯化氢比硫化氢稳定;
⑤稀盐酸不跟铜反应,浓硫酸能跟铜反应;
⑥浓盐酸有挥发性,浓H2SO4无挥发性,
上述中能说明氯元素的非金属性比硫元素强的是( )
①硫酸比次氯酸稳定;
②高氯酸是比硫酸更强的酸;
③S2-易被氯气氧化;
④氯化氢比硫化氢稳定;
⑤稀盐酸不跟铜反应,浓硫酸能跟铜反应;
⑥浓盐酸有挥发性,浓H2SO4无挥发性,
上述中能说明氯元素的非金属性比硫元素强的是( )
| A、①②③ | B、②③④ |
| C、③④⑤ | D、④⑤⑥ |
考点:非金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:从判断元素非金属性强弱的方法:最高价氧化物对应水化物的酸性强弱、与氢气反应的难以程度、气态氢化物的稳定性等.
解答:
解:①硫酸是硫元素的最高价氧化物对应的水化物,但是次氯酸不是元素的最高价氧化物对应的水化物,硫酸比次氯酸稳定不能证明氯元素的非金属性比硫元素强,故错误;
②硫酸是S素的最高价氧化物对应的水化物,高氯酸是Cl的最高价氧化物对应的水化物,高氯酸是比硫酸更强的酸,能说明氯元素的非金属性比硫元素强,故正确;
③S2-易被氯气氧化为硫单质,氯气能置换出单质硫,能说明氯元素的非金属性比硫元素强,故正确;
④根据元素的氢化物越稳定,其元素的非金属性越强的原则知道,氯化氢比硫化氢稳定,能说明氯元素的非金属性比硫元素强,故正确;
⑤稀盐酸不跟铜反应是因为铜排在氢的后面,浓硫酸能跟铜反应是因为浓硫酸具有强氧化性,不能说明氯元素的非金属性比硫元素强,故错误;
⑥浓盐酸有挥发性,浓H2SO4无挥发性,不能说明氯元素的非金属性比硫元素强,故错误;
故选B.
②硫酸是S素的最高价氧化物对应的水化物,高氯酸是Cl的最高价氧化物对应的水化物,高氯酸是比硫酸更强的酸,能说明氯元素的非金属性比硫元素强,故正确;
③S2-易被氯气氧化为硫单质,氯气能置换出单质硫,能说明氯元素的非金属性比硫元素强,故正确;
④根据元素的氢化物越稳定,其元素的非金属性越强的原则知道,氯化氢比硫化氢稳定,能说明氯元素的非金属性比硫元素强,故正确;
⑤稀盐酸不跟铜反应是因为铜排在氢的后面,浓硫酸能跟铜反应是因为浓硫酸具有强氧化性,不能说明氯元素的非金属性比硫元素强,故错误;
⑥浓盐酸有挥发性,浓H2SO4无挥发性,不能说明氯元素的非金属性比硫元素强,故错误;
故选B.
点评:判断元素非金属性强弱的方法:最高价氧化物对应水化物的酸性强弱、与氢气反应的难以程度、气态氢化物的稳定性等,注意知识的归纳和梳理是关键,难度中等.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列试剂的保存方法错误的是( )
| A、钠--煤油中 |
| B、硫磺--二硫化碳中 |
| C、白磷--水中 |
| D、苯酚--隔绝空气,密封保存 |
碳纳米管是近年来材料科学研究的热点.为除去碳纳米管中的杂质--碳纳米颗粒(少量碳原子的聚集体),可以将样品溶解于强酸性的K2Cr2O7溶液中充分反应,当溶液由橙色转变为墨绿色(Cr3+)即可,同时放出一种无毒的气体.以下判断正确的是( )
| A、可以用浓盐酸调节K2Cr2O7溶液的酸性 |
| B、该过程中每氧化2 mol碳纳米颗粒,转移8NA个电子 |
| C、若将该反应设计为原电池,则碳纳米颗粒应作为原电池的正极 |
| D、可以通过过滤的方法最终得到碳纳米管 |
某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液,经测定ClO-与ClO
的浓度之比为1:3,则Cl2与NaOH溶液反应时参加反应的Cl2与被氧化的氯气的物质的量之比为( )
- 3 |
| A、21:5 | B、11:3 |
| C、3:1 | D、5:1 |
根据元素周期律,下列判断正确的是( )
| A、碱性 Mg(OH)2>Ca(OH)2 |
| B、酸性 H2SO4<H2CO3 |
| C、稳定性 H2S>H2Se |
| D、原子半径 S>P |
下列说法正确的是( )
| A、相同质量的热水比冷水含有更多的热量 |
| B、化学反应限度大,该反应的速率也大 |
| C、在相同条件下,分子破裂为原子所吸收的能量与相应原子结合成分子所放出的能量数值相同 |
| D、化石燃料的开采与使用,有利于节能减排与保护环境 |
下列因果关系叙述正确的是( )
| A、纯碱是一种碱,故可用于去油污 |
| B、SiO2能与氢氟酸及碱反应,故SiO2是两性氧化物 |
| C、Na的金属性比Mg强,故可用Na与MgCl2溶液反应制取Mg |
| D、浓硝酸中的HNO3见光会分解,故有时在实验室看到的浓硝酸呈黄色 |
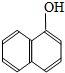
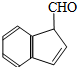
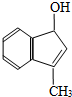
 .下列化合物中,不能与2一奈酚互为同分异构体的是( )
.下列化合物中,不能与2一奈酚互为同分异构体的是( )