题目内容
 实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量铁铝合金与100mL某浓度的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示(C>0).试回答下列问题:
实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量铁铝合金与100mL某浓度的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示(C>0).试回答下列问题:(1)写出反应过程中DE段的离子反应方程式:
(2)合金中,铝的质量为
(3)C的值为
(4)硝酸溶液的物质的量浓度为
考点:化学方程式的有关计算,离子方程式的有关计算
专题:计算题
分析:铝粉和铁粉的混合物与一定量很稀HNO3充分反应,被氧化为Al3+、Fe3+,通过题意,反应始终没有气体生成,可以得出不会有氮的氧化物生成,又有硝酸的浓度越稀,对应还原产物中氮元素的化合价越低,可以推测N元素由+5变成了-3价,由图可得硝酸过量,加入氢氧化钠溶液应先与硝酸反应,再生成沉淀,当沉淀完全后,由图知继续加入氢氧化钠溶液,沉淀量不变,可得与NH4+发生了反应,则随着NaOH的滴加,发生的反应依次有:
①H++OH-=H2O,
②Fe3++3OH-=Fe(OH)3↓,Al3++3OH-=Al(OH)3↓,
③NH4++OH-═NH3?H2O,
④Al(OH)3 +OH-=AlO2-+2H2O
(1)D与E一段沉淀的质量没有发生变化,为NH4NO3和NaOH反应,E与F之间沉淀的量减少,为Al(OH)3溶解在氢氧化钠溶液中,以此书写离子方程式;
(2)根据曲线的变化判断出各段反应,根据消耗的氢氧化钠的体积和反应方程式计算反应后溶液含有铁离子和铝离子的物质的量,再根据原子守恒计算铝和铁的质量;
(3)根据消耗NaOH的总体积,结合在D点氢氧化钠与硝酸、铝铁离子的反应,可计算得出C点氢氧化钠溶液的体积;
(4)根据E点溶液中的溶质结合原子守恒计算硝酸的物质的量浓度.
①H++OH-=H2O,
②Fe3++3OH-=Fe(OH)3↓,Al3++3OH-=Al(OH)3↓,
③NH4++OH-═NH3?H2O,
④Al(OH)3 +OH-=AlO2-+2H2O
(1)D与E一段沉淀的质量没有发生变化,为NH4NO3和NaOH反应,E与F之间沉淀的量减少,为Al(OH)3溶解在氢氧化钠溶液中,以此书写离子方程式;
(2)根据曲线的变化判断出各段反应,根据消耗的氢氧化钠的体积和反应方程式计算反应后溶液含有铁离子和铝离子的物质的量,再根据原子守恒计算铝和铁的质量;
(3)根据消耗NaOH的总体积,结合在D点氢氧化钠与硝酸、铝铁离子的反应,可计算得出C点氢氧化钠溶液的体积;
(4)根据E点溶液中的溶质结合原子守恒计算硝酸的物质的量浓度.
解答:
解:(1)D与E一段沉淀的质量没有发生变化,为NH4NO3和NaOH反应,反应的离子方程式为,NH4++OH-═NH3?H2O,
E与F之间沉淀的量减少,肯定是因为Al(OH)3溶解在氢氧化钠溶液中,反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,
故答案为:NH4++OH-=NH3?H2O;偏铝酸根或四羟基合铝酸根;
(2)E与F之间沉淀的量减少,为Al(OH)3溶解在氢氧化钠溶液中,
其反应方程式为Al(OH)3+NaOH=NaAlO2+2H2O,
氢氧化铝与氢氧化钠物质的量之比为1:1,
EF段的n(NaOH)=4mol/L×2×10-3L=0.008mol,
Al-----Al(OH)3----NaOH→NaAlO2+2H2O
27g 1mol
0.216g 0.008mol
所以铝的质量是0.216g; D与E一段氢氧化钠被消耗,
DE段是NH4NO3和NaOH反应
NH4NO3~NaOH
1 mol 1mol
n(NH4NO3)=n(NaOH)=(34-31)×10-3L×4mol/L=0.012mol,
设铁有xmol,Al离子也是0.008mol,NH4+有0.012mol,根据电子守恒可得:
3x+0.008×3=0.012×8,
x=0.024mol,
所以铁离子有0.024mol,根据原子守恒知,铁的物质的量是0.024mol,其质量=0.024mol×56g/mol=1.344g,
故答案为:0.216;1.344;
(3)滴加NaOH体积为31ml时,
发生反应为①H++OH-=H2O,②Fe3++3OH-=Fe(OH)3↓,Al3++3OH-=Al(OH)3↓,
可计算得出C点氢氧化钠溶液的体积为
31ml-
×103ml/L=7mL.
故答案为:7;
(4)E点时,溶液中的溶质是硝酸钠和氨水,n(NH3?H2O )=n(NH4+)=0.012mol,n(NaNO3)=n(NaOH)=34×10-3L×4mol/L=0.136mol,根据氮原子守恒知,C(HNO3)=
=
=1.48mol/L,
故答案为:1.48.
E与F之间沉淀的量减少,肯定是因为Al(OH)3溶解在氢氧化钠溶液中,反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,
故答案为:NH4++OH-=NH3?H2O;偏铝酸根或四羟基合铝酸根;
(2)E与F之间沉淀的量减少,为Al(OH)3溶解在氢氧化钠溶液中,
其反应方程式为Al(OH)3+NaOH=NaAlO2+2H2O,
氢氧化铝与氢氧化钠物质的量之比为1:1,
EF段的n(NaOH)=4mol/L×2×10-3L=0.008mol,
Al-----Al(OH)3----NaOH→NaAlO2+2H2O
27g 1mol
0.216g 0.008mol
所以铝的质量是0.216g; D与E一段氢氧化钠被消耗,
DE段是NH4NO3和NaOH反应
NH4NO3~NaOH
1 mol 1mol
n(NH4NO3)=n(NaOH)=(34-31)×10-3L×4mol/L=0.012mol,
设铁有xmol,Al离子也是0.008mol,NH4+有0.012mol,根据电子守恒可得:
3x+0.008×3=0.012×8,
x=0.024mol,
所以铁离子有0.024mol,根据原子守恒知,铁的物质的量是0.024mol,其质量=0.024mol×56g/mol=1.344g,
故答案为:0.216;1.344;
(3)滴加NaOH体积为31ml时,
发生反应为①H++OH-=H2O,②Fe3++3OH-=Fe(OH)3↓,Al3++3OH-=Al(OH)3↓,
可计算得出C点氢氧化钠溶液的体积为
31ml-
| 0.032mol×3 |
| 4mol/L |
故答案为:7;
(4)E点时,溶液中的溶质是硝酸钠和氨水,n(NH3?H2O )=n(NH4+)=0.012mol,n(NaNO3)=n(NaOH)=34×10-3L×4mol/L=0.136mol,根据氮原子守恒知,C(HNO3)=
| n(NaNO3)+n(NH3.H2O) |
| V |
| 0.136mol+0.012mol |
| 0.1L |
故答案为:1.48.
点评:本题考查金属与硝酸的反应、氧化还原反应、化学计算等知识点,属于中等难度试题,解答此题关键是判断出硝酸的还原产物以及电子转移守恒的运用.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
下列说法错误的是(NA表示阿伏伽德罗常数的值)( )
A、NA个Fe原子的质量为56g,则1个Fe原子的质量为
| ||
B、20℃时,铝的密度为2.7g?cm-3,则1个Al原子的体积为
| ||
C、4℃时,水的密度为1.0g?cm-3,则1个H2O分子的体积为
| ||
D、标准状况下,NA个N2分子所占的体积约为22.4L,则1个N2分子的体积为
|
下列溶液中溶质的物质的量浓度为1mol?L-1的是( )
| A、将40gNaOH溶解于1L水中配成的NaOH溶液 |
| B、从1000mL1mol/L NaCl溶液中取出100mL的溶液 |
| C、将1L10mol/L的浓盐酸与9L水混合而成的溶液 |
| D、常温常压下将22.4LHCl气体溶于水配成1L的盐酸溶液 |
NA表示阿伏加德罗常数,下列判断正确的是( )
| A、25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| B、常温常压下,22.4LCO2中含有的CO2分子数小于NA个 |
| C、等物质的量的N2和CO的质量均为28g |
| D、常温下,1L 0.1mol/LNa2CO3溶液中,含有阴离子的总数小于0.1NA |
下列物质的核磁共振氢谱图中,吸收峰最少的是( )
A、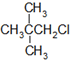 |
B、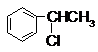 |
C、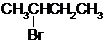 |
D、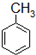 |
