题目内容
17.下列实验操作正确且能达到预期目的是( )| 实验目的 | 操作 | |
| A | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
| B | 欲证明CH2=CHCHO中含有碳碳双键 | 滴入KMnO4酸性溶液,看紫红色是否褪去 |
| C | 检验溴乙烷中的溴原子 | 将溴乙烷与氢氧化钠水溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 |
| D | 制备溴苯 | 苯、溴水和铁屑混合于带长导管的烧瓶中 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.钠与水反应比与乙醇反应剧烈;
B.碳碳双键、-CHO均能被高锰酸钾氧化;
C.水解后检验溴离子,应在酸性条件下;
D.苯与溴水不反应.
解答 解:A.钠与水反应比与乙醇反应剧烈,则分别与Na反应可比较水和乙醇中羟基氢的活泼性强弱,故A正确;
B.碳碳双键、-CHO均能被高锰酸钾氧化,则KMnO4酸性溶液褪色不能检验碳碳双键,故B错误;
C.水解后检验溴离子,应在酸性条件下,应加硝酸至酸性,再加硝酸银溶液检验,故C错误;
D.苯与溴水不反应,苯、液溴和铁屑混合于带长导管的烧瓶中可制备溴苯,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握有机物的结构与性质、有机反应、有机物的制备、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案
相关题目
15.下列说法正确的是( )
| A. | 食用油和鸡蛋清水解都能生成氨基酸 | |
| B. | 乙酸乙酯与乙烯在一定条件下都能与水发生加成反应 | |
| C. | 丙烯分子中最多有8个原子共平面 | |
| D. | 用碳酸钠溶液可以区分乙醇、乙酸、苯和硝基苯四种有机物 |
16.相同温度时 100mL 0.01mol/L 的碳酸钠溶液与 10mL 0.1mol/L 的碳酸钠溶液相比,下列数值前者大于后者的是( )
| A. | OH-的物质的量 | B. | CO32-的物质的量 | C. | c(HCO3-) | D. | 由水电离的 c(OH-) |
5.N2与O2的混合气体的密度对氢气的相对密度为14.5,则N2在混合气体中的质量分数为( )
| A. | 72.4% | B. | 75% | C. | 50% | D. | 80.5% |
2.下列物质不能作为食品添加剂的是( )
| A. | 食盐 | B. | 蔗糖 | C. | 香料 | D. | 福尔马林 |
9.关于硝酸的说法不正确的是( )
| A. | 硝酸与金属反应时,主要是+5价的氮得电子 | |
| B. | 浓HNO3见光易分解,所以应保存在棕色试剂瓶中 | |
| C. | 硝酸电离出的H+离子,能被Zn、Fe等金属还原成H2 | |
| D. | 常温下,向浓⑤中投入Fe片,无明显现象 |
7.下列过程放出热量的是( )
| A. | 冰的融化 | B. | 水的分解 | C. | 硝酸铵溶于水 | D. | 浓硫酸稀释 |
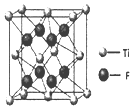 光解水的催化材料可用硝酸镍、硫脲和锐钛矿为原料,采用醇热法制得.
光解水的催化材料可用硝酸镍、硫脲和锐钛矿为原料,采用醇热法制得.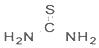 )中C原子轨道的杂化类型为.1mol硫脲中含有σ键的数目为7mol.
)中C原子轨道的杂化类型为.1mol硫脲中含有σ键的数目为7mol.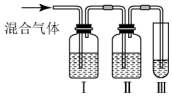 为探究乙烯与溴的加成反应,甲乙两名同学进行如图实验设计:
为探究乙烯与溴的加成反应,甲乙两名同学进行如图实验设计: