题目内容
下列叙述正确的是
A.将稀氨水逐滴加入稀硫酸中,当溶液pH=7,c(SO42-)=c(NH4+)
B.两种醋酸溶液物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2,
C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D.向0.1moL/L的氨水中加入少量硫酸铵固体,则溶液中 增大
增大
C
【解析】
试题分析:A.将稀氨水逐滴加入稀硫酸中,当溶液pH=7,c(SO42-)=2c(NH4+),错误;B.由于醋酸是弱酸,部分电离,在溶液中存在电离平衡,而且浓度越大,电离程度越小。所以两种醋酸溶液物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1>10c2,错误;C.NaOH是强碱,完全电离,pH=11的NaOH溶液c(NaOH)=10-3mol/L;醋酸是弱酸,部分电离,在溶液中存在电离平衡。醋酸溶液pH=3,c(CH3COOH)>10-3mol/L。若二者等体积混合,则由于n(CH3COOH)>n(NaOH),所以溶液显酸性,滴入石蕊溶液呈红色,正确;D.在氨水中存在电离平衡:NH3?H2O NH4++OH-。当向其中加入少量硫酸铵固体时,c(NH4+)增大,平衡逆向移动,c(OH-)的浓度减小,c(NH3?H2O)增大,则溶液中
NH4++OH-。当向其中加入少量硫酸铵固体时,c(NH4+)增大,平衡逆向移动,c(OH-)的浓度减小,c(NH3?H2O)增大,则溶液中 减小,错误。
减小,错误。
考点:考查弱电解质的电离平衡及溶液中离子浓度大小比较的知识。

练习册系列答案
相关题目
 AlCl3
AlCl3 Al
Al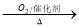 NO
NO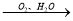 HNO3
HNO3 NaHCO3
NaHCO3 Na2CO3
Na2CO3 SO3
SO3 H2SO4
H2SO4

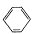

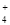 )=c(Cl-)
)=c(Cl-) 2HI(g),在其他条件不变的情况下能增大正反应速率的措施是
2HI(g),在其他条件不变的情况下能增大正反应速率的措施是