题目内容
14.下列有机物名称正确的是( )| A. | 2-乙基戊烷 | B. | 1-甲基--3-乙基苯 | ||
| C. | 2,2-二甲基-4-己烯 | D. | 2-甲基-3-戊炔 |
分析 A、烷烃命名时,要选最长的碳链为主链,从离支链近的一端给主链上碳原子编号,据此分析;
B、苯的同系物在命名时,从简单的侧链开始按顺时针或逆时针给主链上的碳原子进行编号,使侧链的位次和最小;
C、烯烃命名时,要选含官能团的最长的碳链为主链,从离官能团最近的一端给主链上的碳原子编号,并表示出官能团的位置;
D、炔烃命名时,要选含官能团的最长的碳链为主链,从离官能团最近的一端给主链上的碳原子编号,并表示出官能团的位置;
解答 解:A、烷烃命名时,要选最长的碳链为主链,故主链上有6个碳原子,从离支链近的一端给主链上碳原子编号,则在3号碳原子上有一个甲基,故名称为3-甲基己烷,故A错误;
B、苯的同系物在命名时,从简单的侧链开始按顺时针或逆时针给主链上的碳原子进行编号,使侧链的位次和最小,故此有机物应从甲基开始编号,即甲基所在的碳原子为1号,则乙基所在的苯环上的碳原子为3号,故名称为1-甲基-3-乙基苯,故B正确;
C、烯烃命名时,要选含官能团的最长的碳链为主链,故主链上有6个碳原子,从离官能团最近的一端给主链上的碳原子编号,则碳碳双键在2号和3号碳原子之间,在5号碳原子上有2个甲基,故名称为:5,5-二甲基-2-己烯,故C错误;
D、炔烃命名时,要选含官能团的最长的碳链为主链,从离官能团最近的一端给主链上的碳原子编号,故碳碳三键在2号和3号碳原子之间,在4号碳原子上有一个甲基,故名称为:4-甲基-2-戊炔,故D错误;
故选B.
点评 本题考查了烷烃、烯烃、炔烃和苯的同系物的命名,难度不大,注意含官能团的有机物在命名时一切以官能团为首要的考虑对象.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
4.电镀工业会产生大量的电镀污水,处理电镀污水时会产生大量的电镀污泥.电镀污泥含.有多种金属氢氧化物和杂质.下面是处理某种电镀污泥回收铜、镍元素的一种工业流程.
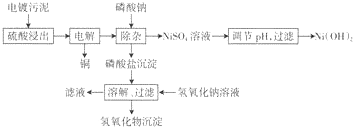
电镀污泥用硫酸浸出后得到的浸出液中各金属离子浓度见下表.
(1)硫酸浸出过程中,为提高浸出速率,可以采取的措施有加热、增大硫酸浓度、搅拌(写出两条).
(2)在电解回收铜的过程中,为提高下一步的除杂效果,需控制电解电压稍大一些使Fe2+氧化,则磷酸盐沉淀中含有的物质为FePO4、CrPO4、AlPO4.
(3)假设电解前后Ni2+浓度基本不变,若使Ni2+在除杂过程不损失,则溶液中P043-浓度不能超过$\sqrt{\frac{5×1{0}^{-31}}{(\frac{7}{59})^{3}}}$mol.L-l.(列出计算表达式,Ksp[Ni3(P04)2]=5xl0-31)
(4)滤液中的Na3PO4可回收循环使用;研究发现当NaOH溶液浓度过大时,部分铝元素和铬元素会在滤液中出现,滤液中出现铝元素的原因为Al(OH)3+OH-=AlO2-+2H2O(用离子方程式解释).
(5)Ni(OH)2是镍氢蓄电池的正极材料,在碱性电解质中,电池充电时Ni(OH)2变为NiOOH,则电池放电时正极的电极反应式为NiOOH+H2O+e-=Ni(OH)2+OH-.
(6)电镀污水中的Cr元素也可以用铁氧体法处理,原理为在废水中加入过量的FeS04,在酸性条件下Cr2072-被还原为Cr3+,同时生成Fe3+;再加入过量的强碱生成铁铬氧体(CrxFe3-xO4)沉淀.写出加入过量强碱生成铁铬氧体( CrxFe3-xO4)沉淀的离子方程式xCr3++Fe2++(2-x)Fe3++8OH-=CrxFe3-xO4↓+4H2O.

电镀污泥用硫酸浸出后得到的浸出液中各金属离子浓度见下表.
| 金属离子 | Cu3+ | Ni3+ | Fe3+ | Al3+ | Cr3+ |
| 浓度(mg/L) | 7000 | 7000 | 2500 | 4200 | 3500 |
(2)在电解回收铜的过程中,为提高下一步的除杂效果,需控制电解电压稍大一些使Fe2+氧化,则磷酸盐沉淀中含有的物质为FePO4、CrPO4、AlPO4.
(3)假设电解前后Ni2+浓度基本不变,若使Ni2+在除杂过程不损失,则溶液中P043-浓度不能超过$\sqrt{\frac{5×1{0}^{-31}}{(\frac{7}{59})^{3}}}$mol.L-l.(列出计算表达式,Ksp[Ni3(P04)2]=5xl0-31)
(4)滤液中的Na3PO4可回收循环使用;研究发现当NaOH溶液浓度过大时,部分铝元素和铬元素会在滤液中出现,滤液中出现铝元素的原因为Al(OH)3+OH-=AlO2-+2H2O(用离子方程式解释).
(5)Ni(OH)2是镍氢蓄电池的正极材料,在碱性电解质中,电池充电时Ni(OH)2变为NiOOH,则电池放电时正极的电极反应式为NiOOH+H2O+e-=Ni(OH)2+OH-.
(6)电镀污水中的Cr元素也可以用铁氧体法处理,原理为在废水中加入过量的FeS04,在酸性条件下Cr2072-被还原为Cr3+,同时生成Fe3+;再加入过量的强碱生成铁铬氧体(CrxFe3-xO4)沉淀.写出加入过量强碱生成铁铬氧体( CrxFe3-xO4)沉淀的离子方程式xCr3++Fe2++(2-x)Fe3++8OH-=CrxFe3-xO4↓+4H2O.
2.已知X、Y、Z、W(含同一元素)有如转化关系,若X是一种单质,W为一种含氧酸,则X不可能是( )
X$\stackrel{O_{2}}{→}$Y$\stackrel{O_{2}}{→}$Z$\stackrel{H_{2}O}{→}$W.
X$\stackrel{O_{2}}{→}$Y$\stackrel{O_{2}}{→}$Z$\stackrel{H_{2}O}{→}$W.
| A. | N2 | B. | C | C. | S | D. | Si |
9.含镁离子和铝离子个数比为1:2的氯化镁和氯化铝两种溶液,若使溶液中的氯离子完全沉淀,用去相同浓度的硝酸银溶液的质量比为( )
| A. | 1:3 | B. | 1:2 | C. | 3:1 | D. | 3:2 |
19.化学与生活密切相关.下列生活中常见物质的俗名与化学式相对应的是( )
| A. | 小苏打--Na2CO3 | B. | 消石灰--Ca (OH)2 | C. | 甲醛--CH3OH | D. | 明矾--KAl(SO4)2 |
3.胶体区别于其它分散系的本质是( )
| A. | 胶体粒子带电荷并且在一定条件下能稳定存在 | |
| B. | 胶体的分散质粒子直径在1nm~100nm之间 | |
| C. | 胶体粒子不能穿过半透膜,能通过滤纸空隙 | |
| D. | 胶体粒子能够发生布朗运动而且能产生丁达尔现象 |
4.设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 44 g CO2 气体中含有原子数为2NA | |
| B. | 常温常压下22.4 L H2 中含原子数为2NA | |
| C. | 64g二氧化硫含有原子数为3NA | |
| D. | 标准状况下22.4 L H2O中含分子数为NA |
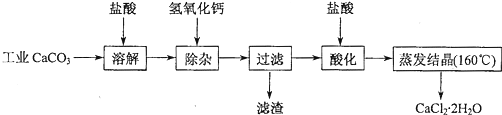
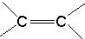 )中的π-键不能自由旋转,因此
)中的π-键不能自由旋转,因此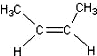 和
和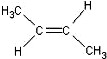 是两种不同的化合物,互为顺反异构体.则分子式为C3H4Cl2的化合物的烯烃异构体有( )
是两种不同的化合物,互为顺反异构体.则分子式为C3H4Cl2的化合物的烯烃异构体有( )