题目内容
16.某同学通过系列实验探究Mg及其化合物的性质,操作正确且能达到目的是( )| A. | 将水加入浓硫酸中得到稀硫酸,置镁条于其中探究Mg的活泼性 | |
| B. | 将NaOH溶液缓慢滴入MgSO4溶液中,观察Mg(OH)2沉淀的生成 | |
| C. | 将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀 | |
| D. | 将镁蒸气在氮气中冷却得到镁粉 |
分析 A、根据稀释浓硫酸应该是把浓硫酸慢慢注入水中分析;
B、根据、氢氧化钠和硫酸镁能够反应产生氢氧化镁沉淀分析;
C、过滤过滤应该用玻璃棒引流分析;
D、氮气与镁反应生成氮化镁.
解答 解:A、稀释浓硫酸应该是把浓硫酸慢慢注入水中,故操作错误,故A错误;
B、氢氧化钠和硫酸镁能够反应产生氢氧化镁沉淀,因此能够观察到沉淀产生,故B正确;
C、过滤应该用玻璃棒引流,而不是直接倒入已装好滤纸的漏斗,故操作错误,故C错误;
D、氮气与镁反应生成氮化镁,所以镁蒸气不能在氮气中冷却得到镁粉,故D错误;
故选:B.
点评 本题主要考查化学实验方案的设计与评价,学会用实验探究物质的性质或变化规律的方法和技巧是解题的关键,能够考查学生的知识运用能力.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
6.CO(g)+H2O(g)?H2(g)+CO2(g)△H<0,在其他条件不变的情况下,下列说法正确的是( )
| A. | 改变压强,平衡不发生移动,反应放出的热量不变 | |
| B. | 加入催化剂,改变了反应的途径,反应的△H也随之改变 | |
| C. | 升高温度,反应速率加快,反应放出的热量不变 | |
| D. | 若在原电池中进行,反应放出的热量不变 |
7.在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)?zC(g),平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的体积扩大两倍,测得A的浓度变为0.35mol/L,下列有关判断正确的是( )
| A. | x+y<z | B. | 平衡正向移动 | C. | B的浓度增大 | D. | A的转化率降低 |
4.以乙烯为原料生产环氧乙烷,经典的方法是氯代乙醇法,包括以下两步反应:
①CH2=CH2+Cl2+H2O→CICH2CH2OH+HCI
②ClCH2CH2OH+HCl+Ca(OH)2→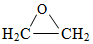 +CaCl2+2H2O
+CaCl2+2H2O
总的反应可表示为:
CH2=CH2+Cl2+Ca(OH)2→ +CaCl2+H2O
+CaCl2+H2O
现代石油化式采用银作催化剂,可一步完成例:
2CH2=CH2+O2 $\stackrel{Ag}{→}$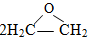
经典的生产工艺的原子利用率是( )
①CH2=CH2+Cl2+H2O→CICH2CH2OH+HCI
②ClCH2CH2OH+HCl+Ca(OH)2→
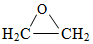 +CaCl2+2H2O
+CaCl2+2H2O总的反应可表示为:
CH2=CH2+Cl2+Ca(OH)2→
 +CaCl2+H2O
+CaCl2+H2O现代石油化式采用银作催化剂,可一步完成例:
2CH2=CH2+O2 $\stackrel{Ag}{→}$

经典的生产工艺的原子利用率是( )
| A. | 12.7% | B. | 25.4% | C. | 50.8% | D. | 76.2% |
11.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 2 g氢气所含原子数为NA | |
| B. | 常温常压下,1.06gNa2CO3含有的Na+离子数为0.02NA | |
| C. | 在常温常压下,11.2LN2所含原子数为NA | |
| D. | 2.7g金属铝和足量盐酸反应,失去的电子数目为0.2NA |
8.关于阿斯匹林的作用叙述中不正确的是( )
| A. | 杀菌消炎 | B. | 解热镇痛 | C. | 防止心脏病发作 | D. | 提高免疫力 |
5.用 NA 表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | T℃1 L pH=6 的纯水中含 10-6 NA个 OH | |
| B. | 6.0 g SiO2 晶体中含有 0.1 NA 个 SiO2分子 | |
| C. | 标准状况下,22.4 L HF 所含电子数为 10NA | |
| D. | 标准状况下,22.4 L 氧气作氧化剂时转移电子数一定为 4NA |
13.下列化学用语表示正确的是( )
| A. | 氯气的电子式:Cl:Cl | |
| B. | 乙烯的结构简式CH2CH2 | |
| C. | 钠原子的结构示意图: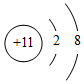 | |
| D. | 硫酸亚铁的电离方程式FeSO4═Fe2++SO42- |