题目内容
10.X、Y、Z是中学化学中常见的单质或化合物,且X、Y、Z均含有同一种元素,它们能实现如下所示的转化关系(其他物质省略):[X]→[Y]$?_{Cu}^{Cl_{2}}$[Z]
(1)若X是一种生活中使用量最大的金属单质,写出Z与Cu反应的离子方程式2Fe3++Cu═2Fe2++Cu2+.
(2)若X是一种非金属单质,常温下为固体;Y是一种能使品红溶液褪色且加热后又能恢复原来颜色的化合物.
写出Z和Cu反应的化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
分析 X、Y、Z是中学化学中常见的单质或化合物,且X、Y、Z均含有同一种元素,
(1)若X是一种生活中使用量最大的金属单质判断为Fe,铁为变价金属元素,Y和氯气反应生成Z证明Y未亚铁盐,Z为铁盐,Z与Cu反应为铁离子氧化铜生成亚铁离子和铜离子;
(2)若X是一种非金属单质,常温下为固体;Y是一种能使品红溶液褪色且加热后又能恢复原来颜色的化合物,判断Y为SO2,则X为S,Z为H2SO4.
解答 解:(1)若X是一种生活中使用量最大的金属单质判断为Fe,铁为变价金属元素,Y和氯气反应生成Z证明Y未亚铁盐,Z为铁盐,Z与Cu反应为铁离子氧化铜生成亚铁离子和铜离子,反应的离子方程式为:2Fe3++Cu═2Fe2++Cu2+,故答案为:2Fe3++Cu═2Fe2++Cu2+;
(2)若X是一种非金属单质,常温下为固体;Y是一种能使品红溶液褪色且加热后又能恢复原来颜色的化合物,判断Y为SO2,则X为S,Z为H2SO4.Z和Cu反应的化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
点评 本题考查无机物的推断,题目难度不大,本题注意根据反应的转化关系结合物质的相关性质为解答的突破口进行推断,牢固把握元素化合物知识是解答该类题目的前提,学习中注意积累.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
20.下列各组物质中,只用溴水一种试剂不能加以区别的是( )
| A. | 苯己烷甲苯 | B. | 硫化氢二氧化硫二氧化碳 | ||
| C. | 苯苯酚乙醇 | D. | 乙烷乙烯乙炔 |
1.亚碳化合物的特征是在1个碳原子上带有2个未成对电子,亚碳化合物是具有很高反应活性的有机化合物.下列属于亚碳化合物的是( )
| A. | CH3 | B. | H2C5(线状) | C. | 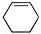 | D. | CH2═CH2 |
18.下列说法正确的是( )
| A. | 水晶项链和餐桌上的瓷盘都是硅酸盐制品 | |
| B. | 新制氯水中的所有物质都是电解质 | |
| C. | 氮氧化物、二氧化硫是形成酸雨的主要物质 | |
| D. | 制造光导纤维的原料是晶体硅 |
5.下列关于化学用语的表示正确的是( )
| A. | 中子数为20的氯(Cl)原子: | B. | CO2的电子式: | ||
| C. | CCl4分子的比例模型: | D. | 镁的离子结构示意图: |
15.下列有关有机化学的说法中正确的是( )
| A. | 除去硬脂酸钠溶液中的甘油方法是:往溶液中加入饱和食盐水,分液 | |
| B. | 治疗疟疾的青蒿素(如图)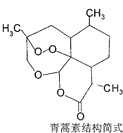 ,分子式是C15H20O5 ,分子式是C15H20O5 | |
| C. | 有机物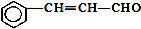 可发生加成反应、氧化反应、还原反应和聚合反应 可发生加成反应、氧化反应、还原反应和聚合反应 | |
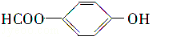
| D. | 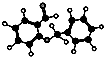 右图所示的有机物分子式为C14H12O2,不能发生银镜反应 右图所示的有机物分子式为C14H12O2,不能发生银镜反应 |
2.下列说法正确的是( )
| A. | 离子交换膜在工业生产中广泛应用,如氯碱工业使用了阴离子交换膜 | |
| B. | 往海带灰的浸泡液中加入过量的氯水,保证I-完全氧化为I2 | |
| C. | 目前科学家已经制得单原子层锗,其电子迁移率是硅的10倍,有望取代硅用于制造更好的晶体管 | |
| D. | 等质量的甲醛与乳酸[CH3CH(OH)COOH]完全燃烧消耗氧气的量不相等 |
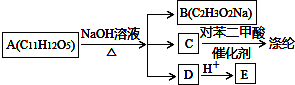


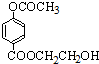 或
或