题目内容
关于2L 0.5mol?L-1的氯化钠溶液,下列说法正确的是( )
| A、溶液中含0.5molNa+ |
| B、58.5g氯化钠溶于水后,配成2000mL溶液 |
| C、58.5g氯化钠溶于2L水中 |
| D、溶液中含0.5molCl- |
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:A.钠离子浓度等于氯化钠的浓度,根据n=cV计算钠离子物质的量;
B.根据n=
计算氯化钠的物质的量,再根据c=
计算判断;
C.58.5g氯化钠的物质的量为1mol,溶于水配成2L溶液,所得溶液浓度为0.5mol/L;
D.氯离子浓度等于氯化钠的浓度,根据n=cV计算氯离子物质的量.
B.根据n=
| m |
| M |
| n |
| V |
C.58.5g氯化钠的物质的量为1mol,溶于水配成2L溶液,所得溶液浓度为0.5mol/L;
D.氯离子浓度等于氯化钠的浓度,根据n=cV计算氯离子物质的量.
解答:
解:A.钠离子浓度为0.5mol/L,故钠离子物质的量=2L×0.5mol/L=1mol,故A错误;
B.氯化钠的物质的量=
=1mol,溶液体积为2L,则溶液物质的量浓度=
=0.5mol/L,故B这正确;
C.58.5g氯化钠的物质的量为1mol,溶于水配成2L溶液,所得溶液浓度为0.5mol/L,体积2L为溶液体积,不是溶剂水的体积,故C错误;
D.氯离子浓度为0.5mol/L,故氯离子物质的量=2L×0.5mol/L=1mol,故D错误;
故选B.
B.氯化钠的物质的量=
| 58.5g |
| 58.5g/mol |
| 1mol |
| 2L |
C.58.5g氯化钠的物质的量为1mol,溶于水配成2L溶液,所得溶液浓度为0.5mol/L,体积2L为溶液体积,不是溶剂水的体积,故C错误;
D.氯离子浓度为0.5mol/L,故氯离子物质的量=2L×0.5mol/L=1mol,故D错误;
故选B.
点评:本题考查物质的量浓度有关计算,比较基础,侧重对基础知识的巩固.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列叙述正确的是( )
| A、锥形瓶可用作加热的反应器 |
| B、室温下,不能将浓硫酸盛放在铁桶中 |
| C、配制溶液定容时,俯视容量瓶刻度会使溶液浓度偏高 |
| D、用蒸馏水润湿的试纸测溶液的pH,一定会使结果偏低 |
下列化学用语正确的是( )
A、NH3分子的电子式: |
B、CH4分子的比例模型: |
| C、乙醇的结构简式:CH3CH2OH |
D、K+离子的结构示意图: |
甲醛(CH2O)、乙酸(C2H4O2)和丙醛(C3H6O)组成的混合物中,氧元素的质量分数是37%,则氢元素的质量分数为( )
| A、11% | B、28% |
| C、54% | D、9% |
有关电化学原理说法中,正确的是( )
| A、在镀件上电镀铜,用铜作阳极 |
| B、电解法精炼粗铜,用粗铜作阴极 |
| C、氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- |
| D、用电解饱和食盐水的方法制取金属钠 |
 某反应的反应过程中能量变化如图所示,(图中E1表示反应的活化能,E2表示活化分子变成生成物分子放出的能量).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示,(图中E1表示反应的活化能,E2表示活化分子变成生成物分子放出的能量).下列有关叙述正确的是( )| A、该反应为放热反应 |
| B、该反应为吸热反应 |
| C、催化剂能改变反应的焓变 |
| D、催化剂能降低反应的活化能 |
下列有关化学用语使用正确的是( )
A、硫离子的结构示意图: | ||
B、NH4Cl的电子式: | ||
C、原子核内有10个中子的氧原子:
| ||
D、Na2O2的电子式为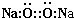 |
大米中含有丰富的维生素B1、B2,应怎样淘米营养素损失少?( )
| A、用热水烫洗 |
| B、浸泡后再流水冲洗 |
| C、用力搓洗 |
| D、根据米的清洁程度适当清洗 |