题目内容
【题目】已知某纯碱(Na2CO3)试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。主要实验步骤如下:
①按图组装仪器,并检查装置的气密性;
②将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;
③称量盛有碱石灰的U型管的质量,得到b g;
④从分液漏斗滴入6mol/L的硫酸,直到不再产生气体时为止;
⑤从导管A处缓缓鼓入一定量的空气;
⑥再次称量盛有碱石灰的U型管的质量,得到c g ;
⑦重复步骤⑤和⑥的操作,直到U型管的质量基本不变,为d g。
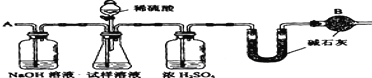
请填空和回答问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明______
①样品重 ②样品轻 ③砝码重 ④砝码轻
(2)装置中干燥管B的作用是______
(3)如果分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果将 _____(填偏高、偏低或不变);如果缺少盛浓硫酸的洗气瓶,测试的结果将______(填偏高、偏低或不变)。
(4)步骤⑤目的是____________。
(5)该试样中纯碱的质量分数的计算式为 ________(结果无须化简)。
【答案】①④ 防止空气中的CO2和水蒸气进入U型管中 偏高 偏高 把反应产生的CO2全部导入U型管中 106(d—b)/44a×100%
【解析】
(1) 根据天平称量时按照左物右码的原则考虑;
(2)根据测定混合物中的碳酸钠,是准确测定和酸反应生成的二氧化碳气体的量,避免空气中的二氧化碳进入考虑;因为空气中也有二氧化碳和水分,干燥管B的作用就是不让它们进入的;
(3)根据盐酸的挥发性考虑;根据浓硫酸洗气瓶的作用考虑;
(4)因为反应完了锥形瓶中存留有二氧化碳,鼓入一定量的空气就是为了驱赶它们的;
(5)根据U型管的质量的增加量就是生成的二氧化碳的质量,根据二氧化碳的质量算出碳酸钠的质量,再用碳酸钠的质量除以样品质量即可。
(1) 由于称量时左物右码,向左偏说明样品重,砝码轻,选①④,
因此,本题正确答案是:①④;
(2)U型管中的碱石灰是为了吸收反应生成的二氧化碳,但空气中也存在二氧化碳,干燥管B的作用就是防止空气中的二氧化碳和水分进入U型管,对结果产生误差,
因此,本题正确答案是:防止空气中的CO2和水蒸气进入U型管中;
(3)因为盐酸具有挥发性,也会随着二氧化碳进入U型管,被误认为是二氧化碳,所以二氧化碳的质量偏大,算出的碳酸钠的质量也会偏大的,所以结果会偏高;浓硫酸的作用是吸水,如果缺少盛浓硫酸的洗气瓶,水蒸气也进入U型管被吸收,算出的碳酸钠的质量也会偏大的,所以结果会偏高,
因此,本题正确答案是:偏高;偏高;
(4)因为反应完了锥形瓶中存留有二氧化碳,鼓入一定量的空气就是将残留的二氧化碳完全排入U型管;
因此,本题正确答案是:把反应产生的CO2全部导入U型管中;
(5)设需要碳酸钠的质量为X则:
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
106 44
X d-b
列比例式:![]() =
=![]()
计算得出X=![]() ;
;
所以试样中纯碱的质量分数的计算式为106(d—b)/44a×100%,
因此,本题正确答案是:106(d—b)/44a×100%。