题目内容
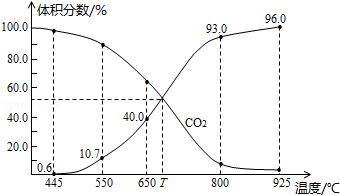
13.一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示:已知气体分压(P分)=气体总压(P总)×体积分数,下列说法不正确的是( )
| A. | 550℃时,若充入惰性气体,v正,v逆均减小 | |
| B. | 650℃时,反应达平衡后CO2的转化率为25.0% | |
| C. | T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动 | |
| D. | 925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=23.04P总 |
分析 A、可变的恒压密闭容器中反应,550℃时若充入惰性气体,相当于减小压强,则v正,v退均减小,又改反应是气体体积增大的反应,则平衡正向移动;
B、由图可知,650℃时,反应达平衡后CO的体积分数为40%,设开始加入的二氧化碳为1mol,根据三段式进行计算;
C、由图可知,T℃时,反应达平衡后CO和CO2的体积分数都为50%即为平衡状态;
D、925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=$\frac{p(CO)^{2}}{p(C{O}_{2})}$,据此计算.
解答 解:A、可变的恒压密闭容器中反应,550℃时若充入惰性气体,相当于减小压强,则v正,v退均减小,故A正确;
B、由图可知,650℃时,反应达平衡后CO的体积分数为40%,设开始加入的二氧化碳为1mol,转化了xmol,
则有C(s)+CO2(g)?2CO(g)
开始 1 0
转化 x 2x
平衡; 1-x 2x
所以$\frac{2x}{1-x+2x}$×100%=40%,解得x=0.25mol,则CO2的转化率为$\frac{0.25}{1}$×100%=25%,故B正确;
C、由图可知,T℃时,反应达平衡后CO和CO2的体积分数都为50%即为平衡状态,所以平衡不移动,故C错误;
D、925℃时,CO的体积分数为96%,则CO2的体积分数都为4%,所以用平衡分压代替平衡浓度表示的化学平衡常数Kp=$\frac{p(CO)^{2}}{p(C{O}_{2})}$=$\frac{(0.96p)^{2}}{0.04p}$=23.04P,故D正确;
故选:C.
点评 本题考查了化学平衡图象、阅读题目获取信息的能力等,难度中等,需要学生具备运用信息与基础知识分析问题、解决问题的能力.

| A. | 钠和钾的合金在常温下呈液态,通常用作原子反应堆的导热剂 | |
| B. | 氢的两种同位素氘和氚可用来作氢弹 | |
| C. | 为了观察氢气燃烧时的火焰颜色,可将玻璃导管换成石英管 | |
| D. | 56度的二锅头白酒中乙醇的质量分数为56% |
| A. | 用核磁共振氢谱不能鉴别1-丙醇和2-丙醇 | |
| B. | 实验证实 可使Br2的CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 可使Br2的CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 | |
| C. | 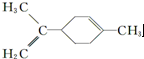 所有碳原子一定在同一平面上 所有碳原子一定在同一平面上 | |
| D. | 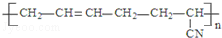 的单体是CH3-C≡C-CH3和CH2═CH-CN 的单体是CH3-C≡C-CH3和CH2═CH-CN |
| A. | 溶解度(25℃):小苏打<苏打 | B. | 沸点:H2Se>H2S>H2O | ||
| C. | 密度:溴乙烷>水 | D. | 碳碳键键长:乙烯<苯 |
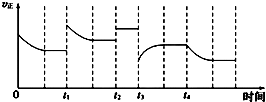 合成氨反应:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,在反应过程中,正反应速率的变化如图,下列说法中正确的是( )
合成氨反应:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,在反应过程中,正反应速率的变化如图,下列说法中正确的是( )| A. | t1时升高了温度 | |
| B. | t2时恒压条件下加入了惰性气体 | |
| C. | t3时增大了压强 | |
| D. | t2、t3、t4三个时刻中t4时NH3的百分含量最低 |
| A. | 热稳定性:H2O>H2S | B. | 酸性:HCl>H2CO3 | ||
| C. | 金属性:K>Li | D. | 碱性:NaOH>Mg(OH)2 |
| A. | 金属钠与TiCl4溶液反应,可以置换出金属钛 | |
| B. | 氢氧化铝具有弱碱性,可用于做胃酸中和剂 | |
| C. | 漂白粉在空气中不稳定,可用于漂白纸张 | |
| D. | 氧化铁能与酸反应,可用于制作红色涂料 |

| A. | 该有机物属于芳香烃 | |
| B. | 该物质不能使酸性高锰酸钾溶液褪色 | |
| C. | 该分子对称性好,所以没有顺反异构 | |
| D. | 该有机物分子中,最多可能有18个碳原子共平面 |