题目内容
13.己知aX+和bY-具有与氖原子相同的电子层结构,下列关系正确的是( )| A. | 质子数:a>b | B. | 离子半径:r(aX+)>r(bY-) | ||
| C. | X、Y可形成XY2型化合物 | D. | 原子半径:r(Y)>r(X) |
分析 aX+和bY-具有与氖原子相同的电子层结构,则X的原子序数=10+1=11,为Na元素;Y的原子序数=10-1=9,为F元素,据此结合元素周期律知识进行判断.
解答 解:aX+和bY-具有与氖原子相同的电子层结构,则X的原子序数=10+1=11,为Na元素;Y的原子序数=10-1=9,为F元素,
A.Na的质子数为11,F的质子数为9,则质子数:a>b,故A正确;
B.aX+和bY-具有与氖原子相同的电子层结构,原子序数越大离子半径越小,则离子半径:r(aX+)<r(bY-),故B正确;
C.Na与F形成的化合物为NaF,为XY型化合物,故C错误;
D.Na含有3个电子层,F含有2个电子层,电子层越多原子半径越大,则原子半径:r(Y)<r(X),故D错误;
故选A.
点评 本题考查半径比较、核外电子排布、结构与位置关系,题目难度不大,判断X、Y的位置关系是关键,要灵活运用元素周期律知识解答,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
13.下列关于家庭常备药物阿司匹林和扑热息痛的描述不正确的是( )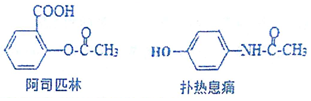

| A. | FeCl3溶液可鉴别阿斯匹林和扑热息痛 | |
| B. | 1mol阿斯匹林最多可消耗2mol的NaOH | |
| C. | 在一定条件,扑热息痛可与HCHO发生缩聚反应 | |
| D. | 二者都能发生水解反应 |
1.在一定条件下的定容密闭容器中反应:A(s)+2B(g)?C(g)+D(g),当下列物理量不再变化时,不能表明该反应已达平衡的是( )
| A. | 混合气体的压强 | B. | 混合气体的密度 | ||
| C. | B的物质的量浓度 | D. | 混合气体的平均相对分子质量 |
18.下列关于吸热反应的分析正确的是( )
| A. | 生成物化学键形成时也会吸收热量 | |
| B. | 生成物的总能量高于反应物的总能量 | |
| C. | 一定需要加热条件下才能实现 | |
| D. | 使用催化剂可以降低吸热反应的热效应 |
5.表是某城市空气质量每周公报的部分内容.下列选项中不会对表中3个空气质量指标产生影响的是( )
| 项目 | 空气污染指数(API) | 空气质量级别 | 空气质量描述 |
| 总悬浮颗粒 | 52 | Ⅱ | 良 |
| 二氧化硫 | 7 | I | 优 |
| 二氧化氮 | 24 | I | 优 |
| A. | 用煤和石油产品作燃料 | B. | 汽车排放的尾气 | ||
| C. | 使用含磷洗衣粉 | D. | 焚烧垃圾 |
2.关于溶液的下列说法正确的是( )
| A. | 等体积、对物质的量浓度的NaX和弱酸HX混合后的溶液中:C(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) | |
| B. | 等物质的量浓度的下列溶液:①H2CO3②Na2CO3③NaHCO3④(NH4)2CO3中c(CO32-)的大小关系为:②>④>③>① | |
| C. | 往0.1mol/L CH3COOH溶液中通入少量HCl,醋酸的电离平衡向逆反应方向移动,且溶液中$\frac{c(C{H}_{3}COOH)}{c({H}^{+})•c(C{H}_{3}CO{O}^{-})}$增大 | |
| D. | Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
3.下列对有机化合物用途的说法中,正确的是( )
| A. | 医用消毒酒精的体积分数为95% | |
| B. | 常用福尔马林溶液保存动物标本 | |
| C. | 医院常用银氨溶液检验病人的尿糖 | |
| D. | 工业上常用乙烷和氯气反应制取氯乙烷 |

 .
.