题目内容
下列过程表达式中,属于电离方程式的是( )
| A、HCO3-+H2O?H2CO3+OH- |
| B、HS-+H2O?S2-+H3O+ |
| C、NH3+H+=NH4+ |
| D、HSO3-+OH-=H2O+SO32- |
考点:电离方程式的书写
专题:离子反应专题
分析:电离方程式是表示物质电离的式子,强电解质完全电离,用等号表示,弱电解质部分电离,用可逆号表示.
解答:
解:A、是碳酸氢根水解的方程式,故A错误;
B、H2S是弱酸,不完全电离,用可逆号,而且电离分两步进行,该式子是H2S的第二步电离方程式,故B正确;
C、是氨气和强酸反应的离子方程式,故C错误;
D、是亚硫酸氢根离子和氢氧根离子反应的化学方程式,故D错误.
故选B.
B、H2S是弱酸,不完全电离,用可逆号,而且电离分两步进行,该式子是H2S的第二步电离方程式,故B正确;
C、是氨气和强酸反应的离子方程式,故C错误;
D、是亚硫酸氢根离子和氢氧根离子反应的化学方程式,故D错误.
故选B.
点评:本题考查学生电离方程式的书写和判断知识,属于基本知识的考查,难度不大.

练习册系列答案
相关题目
已知一定温度下2X(g)+Y (g)?mZ(g)△H=-a kJ?mol-1 (a>0),现有甲乙两容积相等且固定不变的密闭容器,在保持该温度下,向密闭容器甲中通入2molX和1molY,达到平衡状态时,放出热量bkJ;向密闭容器乙中通入1molX和0.5molY,达到平衡状态时,放出热量ckJ,且b>2c,则a、b、m的值或关系正确的是( )
| A、m=4 | B、a=b |
| C、b<a | D、m等于2或1 |
如图所示的原电池,下列叙述正确的是(盐桥中装有含琼胶的KCl饱和溶液)( )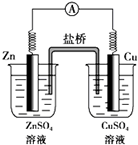

| A、反应中,盐桥中的Cl-会移向ZnSO4溶液 |
| B、取出盐桥后,电流计依然发生偏转 |
| C、铜片上有气泡逸出 |
| D、锌为负极,发生还原反应,电极反应式为:Zn-2e-=Zn2+ |
有关化学用语不正确的是( )
| A、CO2分子的结构式:O=C=O | ||
B、O-18的原子符号:
| ||
C、S2-离子的结构示意图: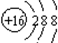 | ||
D、氯化氢分子的电子式: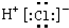 |
下列方程式书写不正确的是( )
| A、NaHS水解:HS-+H2O?H2S+OH- |
| B、氢氧化钡溶于水电离:Ba(OH)2═Ba2++2OH- |
| C、醋酸溶于水电离:CH3COOH?CH3COO-+H+ |
| D、碳酸钠水解:CO32-+2H2O?2OH-+H2CO3 |
某温度下,向容积为20L的密闭反应器中充入0.2molHI(g),达到平衡后测得HI的转化率为80%,则该温度下反应H2(g)+I2(g)?2HI(g)的平衡常数是( )
| A、2.5×10-2 |
| B、0.25 |
| C、4.0 |
| D、4.0×102 |
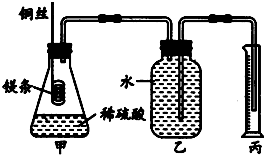 化学兴趣小组设计测定镁原子的摩尔质量的实验,简易装置如图,除去表面氧化膜的镁条质量为0.24g,镁条完全反应后,用量筒收集水,体积为0.224L(设已折换成标准状况下的对应的气体体积).
化学兴趣小组设计测定镁原子的摩尔质量的实验,简易装置如图,除去表面氧化膜的镁条质量为0.24g,镁条完全反应后,用量筒收集水,体积为0.224L(设已折换成标准状况下的对应的气体体积).