题目内容
NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、23g Na在空气中加热完全变成Na2O2,失去NA个电子 |
| B、标准状况下,22.4L H2O含有NA个H2O分子 |
| C、1mol/L的硝酸钠溶液中含有的硝酸根离子数为NA |
| D、0.5mol KClO3中含有Cl-的数目为0.5NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.钠为1价金属,23g钠的物质的量为1mol,完全反应失去1mol电子;
B.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
C.缺少硝酸钠溶液的体积,无法计算溶液中硝酸根离子的数目;
D.氯酸钾在溶液中电离出钾离子和氯酸根离子,溶液中不存在氯离子.
B.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
C.缺少硝酸钠溶液的体积,无法计算溶液中硝酸根离子的数目;
D.氯酸钾在溶液中电离出钾离子和氯酸根离子,溶液中不存在氯离子.
解答:
解:A.23g钠的物质的量为1mol,1mol钠完全反应失去1mol电子,失去NA个电子,故A正确;
B.标况下,水不是气体,不能使用标况下的气体摩尔体积计算22.4L水的物质的量,故B错误;
C.没有告诉硝酸钠溶液的体积,无法计算溶液中硝酸根离子的物质的量及数目,故C错误;
D.氯酸钾在溶液中电离出钾离子和氯离子,不存在氯离子,故D错误;
故选A.
B.标况下,水不是气体,不能使用标况下的气体摩尔体积计算22.4L水的物质的量,故B错误;
C.没有告诉硝酸钠溶液的体积,无法计算溶液中硝酸根离子的物质的量及数目,故C错误;
D.氯酸钾在溶液中电离出钾离子和氯离子,不存在氯离子,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标准状况下水、四氯化碳、乙醇、三氧化硫等不是气体,要求学生掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项C为易错点,注意题中缺少溶液的体积.

练习册系列答案
相关题目
下列有关原子结构和元素周期律的表述正确的是( )
①原子序数为15的元素的最高化合价为+3
②第ⅦA族元素是同周期中非金属性最强的元素
③第ⅥA族元素的原子最高正价等于主族序数
④原子序数为12的元素位于元素周期表的第三周期第ⅡA族.
①原子序数为15的元素的最高化合价为+3
②第ⅦA族元素是同周期中非金属性最强的元素
③第ⅥA族元素的原子最高正价等于主族序数
④原子序数为12的元素位于元素周期表的第三周期第ⅡA族.
| A、①② | B、①③ | C、②④ | D、③④ |
将agNa加入到一定量的稀H2SO4中,使两者恰好完全反应,得到b升气体(标况下),所得溶液中共有C个溶质的离子,阿伏伽德罗常数为NA,则下列关系式正确的是( )
A、NA=
| ||||
B、NA=
| ||||
C、
| ||||
| D、以上均不正确 |
下列热化学方程式或离子方程式中,正确的是( )
| A、甲烷的标准燃烧热为-890.3kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ?mol-1 | |||
B、500℃、30MPa下,将0.5mol N2和1.5mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)
| |||
| C、氯化镁溶液与氨水反应:Mg2++2OH-═Mg(OH)2↓ | |||
| D、氧化铝溶于NaOH溶液:Al2O3+2OH-+3H2O═2Al(OH)3 |
下列有关晶体的叙述中,正确的是( )
| A、在CaF2晶体中,Ca2+、F-的配位数均为8 |
| B、C60晶体中,微粒之间通过共价键结合形成晶体,键角为120° |
| C、在CsCl晶体中,每个Cs+周围紧邻6个Cl- |
| D、金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 |
在以下四种溶液中,各离子一定能大量共存的是( )
| A、滴加酚酞试液显红色的溶液:Fe3+、NH4+、Cl-、CO32- |
| B、含溶质为MgCl2的溶液:K+、NO3-、SO42-、Al3+ |
| C、水电离出来的c(H+)=10-13mol/L的溶液:K+、Na+、HCO3-、Br- |
| D、pH=1的溶液:Fe2+、Na+、I-、NO3- |
下列有关除杂的实验操作合理的是( )
| A、除去二氧化碳中混有的少量一氧化碳:通入适量氧气后点燃 |
| B、除去氧气中少量氮气:使气体通过炽热的铜粉 |
| C、除去石英中少量碳酸钙:用稀盐酸溶解后过滤 |
| D、除去氯化钠固体中少量的纯碱:加入足量氯化钙,过滤、蒸发、结晶 |
它们的氯化物的化学式,最可能正确的是( )
| A、QCl2 |
| B、RCl3 |
| C、SCl2 |
| D、TCl |
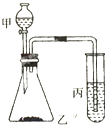 某课外学习小组的同学欲验证碳、硅、硫的非金属性强弱,并给出下列的试剂供选择实验试剂:①浓盐酸、②稀H2SO4、③饱和Na2SO3溶液、④大理石、⑤Na2CO3粉末、⑥Na2SiO3溶液.实验装置如图所示:
某课外学习小组的同学欲验证碳、硅、硫的非金属性强弱,并给出下列的试剂供选择实验试剂:①浓盐酸、②稀H2SO4、③饱和Na2SO3溶液、④大理石、⑤Na2CO3粉末、⑥Na2SiO3溶液.实验装置如图所示: