题目内容
在有乙离子存在时,欲用丙试剂检验溶液中是否含有甲离子,下表所加丙试剂能够对甲离子成功检验的是(不允许加热、过滤、萃取等操作)( )
| 选项 | 甲离子 | 乙离子 | 丙试剂 | ||||
| A | SO
|
SO
|
稀盐酸、Ba(NO3)2的混合溶液 | ||||
| B | Cl- | CO
|
AgNO3溶液、稀硝酸 | ||||
| C | Mg2+ | Al3+ | NaOH溶液 | ||||
| D | Fe2+ | Fe3+ | KSCN溶液 |
| A、A | B、B | C、C | D、D |
分析:A.硝酸根和氢离子在一起具有稀硝酸的性质,有强氧化性,可将SO32-氧化为SO42-;
B.碳酸银溶于硝酸,氯化银不溶;
C.过量氢氧化钠与Mg2+反应生成氢氧化镁沉淀,与Al3+反应不生成沉淀;
D.KSCN与Fe3+反应,溶液呈红色,不能判断是否含有Fe2+.
B.碳酸银溶于硝酸,氯化银不溶;
C.过量氢氧化钠与Mg2+反应生成氢氧化镁沉淀,与Al3+反应不生成沉淀;
D.KSCN与Fe3+反应,溶液呈红色,不能判断是否含有Fe2+.
解答:解:A.硝酸根和氢离子在一起具有稀硝酸的性质,有强氧化性,可将SO32-氧化为SO42-,与钡离子结合生成硫酸钡沉淀,无法确定是否含有SO42-,故A错误;
B.碳酸银溶于硝酸,氯化银不溶,所以加AgNO3溶液和稀硝酸,有白色沉淀,说明含有Cl-,故B正确;
C.过量氢氧化钠与Mg2+反应生成氢氧化镁沉淀,与Al3+反应生成偏铝酸钠溶液,所以加入过量NaOH,如有沉淀生成,可确定含有Mg2+,故C正确;
D.KSCN与Fe3+反应,溶液呈红色,不能判断是否含有Fe2+,故D错误.
故选BC.
B.碳酸银溶于硝酸,氯化银不溶,所以加AgNO3溶液和稀硝酸,有白色沉淀,说明含有Cl-,故B正确;
C.过量氢氧化钠与Mg2+反应生成氢氧化镁沉淀,与Al3+反应生成偏铝酸钠溶液,所以加入过量NaOH,如有沉淀生成,可确定含有Mg2+,故C正确;
D.KSCN与Fe3+反应,溶液呈红色,不能判断是否含有Fe2+,故D错误.
故选BC.
点评:本题考查物质的检验及鉴别,题目难度一般,本题注意把握相关物质的性质以及反应现象.

练习册系列答案
相关题目
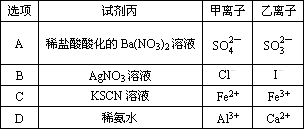
见下表,欲用一种试剂乙来检验(在实验过程中不允许加热、过滤、萃取……等操作)其溶液中的离子X,在同时有离子Y存在时,此检验仍可进行的是( )
|
|
试剂乙 |
离子X |
离子Y |
|
A |
HCl,BaCl2 |
SO |
S2O |
|
B |
NH3·H2O |
Al3+ |
Ag+ |
|
C |
AgNO3 |
I- |
Cl- |
|
D |
NH4SCN |
Fe2+ |
Fe3+ |
见下表,欲用一种试剂乙来检验(在实验过程中不允许加热、过滤、萃取……等操作)其溶液中的离子X,在同时有离子Y存在时,此检验仍可进行的是( )
|
|
试剂乙 |
离子X |
离子Y |
|
A |
HCl,BaCl |
SO |
S2O |
|
B |
NH3·H2O |
Al3+ |
Ag+ |
|
C |
AgNO3 |
I- |
Cl- |
|
D |
NH4SCN |
Fe2+ |
Fe3+ |
在有乙离子存在时,欲用丙试剂检验溶液中是否含有甲离子,下表所加丙试剂能够对甲离子成功检验的是(不允许加热、过滤、萃取等操作)
选项 | 甲离子 | 乙离子 | 丙试剂 |
A |
|
| 稀盐酸、Ba(NO3)2的混合溶液 |
B | Cl- |
| AgNO3溶液、稀硝酸 |
C | Mg2+ | Al3+ | NaOH溶液 |
D | Fe2+ | Fe3+ | KSCN溶液 |