题目内容
9. 氨既是实验室中常用试剂,也是工业上重要原料.
氨既是实验室中常用试剂,也是工业上重要原料.(1)写出实验室制取氨气的化学方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O;
(2)氨在氧气中燃烧,生成水和一种单质.
已知:N2(g)+3H2(g)=2NH3(g)△H=-92.4kJ•mol-1
2H2(g)+O2(g)=2H2O(l)△H=-572kJ•mol-1
写出氨在氧气中燃烧生成液态水和气态单质的热化学方程式:4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H=-1531.2kJ•mol-1;
(3)已知在一定条件下,将2molN2和2molH2混合于一个4L的密闭容器中发生的反应为N2+3H2$?_{高温高压}^{催化剂}$2NH3,5min后达到平衡,平衡时氨的体积分数为25%.
①该反应的平衡常数K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$;
②从反应开始到平衡时,N2的反应速率C(N2)=0.008mol/(L﹒min);
(4)工业上以氨气、空气为主要原料制取硝酸.在容积恒定的密闭容器中进行反应2NO(g)+O2(g)?2NO2(g)△H>0.该反应的反应速率(v)随时间(t)变化的关系如图所示.若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号)AB.
A.在t1-t2时,可依据容器内气体的压强保持不变判断反应已达到平衡状态
B.在t2时,采取的措施可以是升高温度
C.在t3-t4时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
D.在t5时,容器内NO2的体积分数是整个过程中的最大值.
分析 (1)实验室用氯化铵与氢氧化钙加热制取氨气;
(2)①N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1
②2H2(g)+O2(g)═2H2O(l)△H=-572kJ•mol-1
依据盖斯定律②×3-①×②得:4NH3(g)+3O2(g)=2N2(g)+6H2O(l),据此书写热化学方程式;
(3)①化学平衡常数是平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值;
②设参加反应的氮气的物质的量,利用三段法求出各自的物质的量,再根据体积分数求出未知数,然后根据v=$\frac{△c}{△t}$计算反应速率;
(4)2NO(g)+O2(g)?2NO2(g))△H>0.该反应是气体体积减小的吸热反应;
A、压强不变说明反应达到平衡;
B、反应是吸热反应升温正逆反应速率增大,平衡正向进行;
C、反应中气体质量守恒,体积不变,过程中密度不变;
D、依据图象分析器内NO2的体积分数在t3~t4时最大.
解答 解:(1)实验室用氯化铵与氢氧化钙加热制取氨气,反应方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O,
故答案为:Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O;
(2)①N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1
②2H2(g)+O2(g)═2H2O(l)△H=-572kJ•mol-1
依据盖斯定律②×3-①×②得:4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H=-1531.2 kJ•mol-1,
故答案为:4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H=-1531.2 kJ•mol-1;
(3)①该反应的平衡常数表达式K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$,故答案为:$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$;
②设参加反应的氮气的物质的量xmol,
N2+3H2?2NH3
开始(mol):1 3 0
变化(mol):x 3x 2x
平衡(mol):1-x 3-3x 2x
5min后达到平衡,平衡时氨的体积分数=$\frac{2x}{1-x+3-3x+2x}$×100%=25%;
解得x=0.4,
N2的反应速率v(N2)=$\frac{△c}{△t}$=$\frac{\frac{0.4mol}{10L}}{5min}$=0.008mol/(L﹒min);
故答案为:0.008mol/(L﹒min);
(4)A.该反应正反应是气体物质的量减小的反应,恒温恒容下条件下,压强不变,说明到达平衡,故A正确;
B.正反应是放热反应,升高温度平衡向逆反应移动,在t2时,正、逆速率都增大,且正反应速率增大更多,平衡向正反应移动,该反应正反应是气体体积减小的反应,增大压强平衡向正反应进行,转化率增大,故B正确;
C.恒容条件下,反应混合气体的总质量不变,密度始终不变,所以不能说明反应达到平衡状态,故C错误;
D.由图可知,在t2时,改变条件平衡向正反应移动,t3时到达平衡,t4时瞬间正反应速率不变,逆反应速率减小,平衡向正反应进行,应是NO2降低的浓度,故容器内NO2的体积分数在t3时值的最大,故D错误;
故选AB.
点评 本题为综合题,考查了氨气的制备和性质的检验,盖斯定律求反应热,化学平衡的移动及平衡状态的判断,氧化还原方程式的书写,题目难度大,熟悉平衡状态的影响因素是解题关键.

| A. | 氯化亚铁溶液中通入氯气:2Fe2++Cl2═2Fe3++2Cl- | |
| B. | 碳酸钙溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O |
| A. | MgO | B. | CO2 | C. | NH4Cl | D. | N2 |
| A. | 氢氧化铝可用于治疗胃酸过多 | |
| B. | ClO2用于饮用水消毒 | |
| C. | 水玻璃浸泡过的木材既能防腐又能耐火 | |
| D. | Si用于制造光导纤维 |
| A. | 钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 氧化钠与盐酸:O2-+2H+═H2O | |
| C. | 碳酸氢钠溶液与稀硫酸:CO32-+2H+═H2O+CO2↑ | |
| D. | 烧碱溶液与碳酸氢钠溶液:HCO3-+OH-═H2O+CO2↑ |
| A. | 增加Fe的物质的量 | |
| B. | 将容器的体积缩小一半 | |
| C. | 保持体积不变,充入水蒸气 | |
| D. | 压强不变,充入Ne使容器的体积增大 |
| 选项 | 目的 | 试剂或试验方法 | 说明 |
| A | 从苯中提溴 | 加CCl4 | 溴易溶于CCl4 |
| B | 检验含Fe3+溶液中是否含Fe2+ | 加高锰酸钾溶液 | 溶液紫色褪去,说明含Fe2+ |
| C | 配置1mol/LFeCl3溶液100mL | 将一定质量FeCl3溶液转移至容量瓶中加水定容 | 容量瓶规格须为100mL |
| D | 制取漂白粉 | 将氯气通入澄清石灰水中 | 氯气与氢氧化钙反应生成次氯酸钙 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 滴定管和锥形瓶在使用前要用润洗 | |
| B. | 检验红砖中的红色物质是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液 | |
| C. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗上口倒出 | |
| D. | 将CO2和SO2混合气体分别通入BaC12溶液、Ba(NO3)2溶液中,最终都有沉淀生成 |
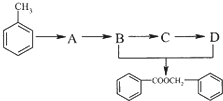
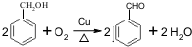 .
. 的化学方程式为
的化学方程式为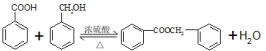 .
.