题目内容
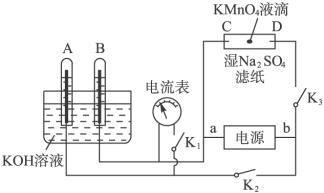
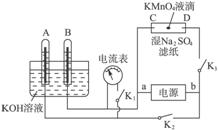
阿波罗宇宙飞船使用氢氧燃料电池,在两极分别通入氢气和氧气,以KOH溶液为电解质溶液,电池工作时总的化学反应可以表示为2H2+O2====2H2O,反应保持在高温下,以使生成的水不断蒸发。下列对阿波罗氢氧燃料电池的论述正确的是( )A.在正极通入氢气,负极通入氧气
B.正极发生的电极反应为H2-2e-====2H+
C.电池的负极发生氧化反应,正极发生还原反应
D.电池工作过程中溶液pH不断增大
解析:根据总方程式2H2+O2====2H2O,在正极通入氧气,O2+4H++4e-====2H2O,发生还原反应;在负极通入氢气,2H2+4OH--4e-====4H2O,发生氧化反应。电池工作过程中,理论上电解质溶液(KOH溶液)没有变化,生成的水不断蒸发,pH应不变化。
答案:C

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
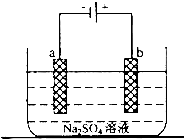 (1)阿波罗宇宙飞船使用的是碱性氢氧燃料电池,负极贮存的是氢气,正极贮存的是氧气,电解质是NaOH溶液.请写出该反应发生的电极反应式.
(1)阿波罗宇宙飞船使用的是碱性氢氧燃料电池,负极贮存的是氢气,正极贮存的是氧气,电解质是NaOH溶液.请写出该反应发生的电极反应式.