题目内容
相对分子质量为M的某物质在室温下的溶解度为Sg水,此时测得饱和溶液的密度为dg/cm3,则该饱和溶液的物质的量浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:物质的量浓度的相关计算
专题:
分析:该饱和溶液的质量分数为:ω=
×100%,然后根据溶质质量分数与物质的量浓度的关系c=
计算出该饱和溶液的物质的量浓度.
| S |
| 100+S |
| 1000ρω |
| M |
解答:
解:该物质在室温下的溶解度为Sg水,则该饱和溶液的质量分数为:ω=
×100%,
该饱和溶液的物质的量浓度为:c=
=
mol/L=
mol/L,所以C正确,
故选C.
| S |
| 100+S |
该饱和溶液的物质的量浓度为:c=
| 1000ρω |
| M |
1000d×
| ||
| M |
| 1000dS |
| M(100+S) |
故选C.
点评:本题考查了物质的量浓度与溶质质量分数的计算,题目难度中等,注意掌握物质的量浓度与溶质质量分数的转化关系式,试题培养了学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
下列有关环境保护的说法不正确的是( )
| A、防止化石燃料燃烧产生的二氧化硫和汽车尾气中的氮氧化物对大气的污染,是改善大气质量的重要任务 |
| B、生活废水中含氮、磷等元素,过多排放会引起水体污染 |
| C、对煤等燃料进行脱硫处理后,可减少燃烧产物中SO2的含量 |
| D、汽车使用乙醇汽油不会排放有害气体,故不必安装尾气净化装置 |
温度相同、浓度均为0.2mol?L-1的 ①(NH4)2SO4、②KNO3、③NH4HSO4、④NH4NO3、⑤NaClO溶液,它们的pH值由小到大的排列顺序是( )
| A、③①④②⑤ |
| B、①③⑤④② |
| C、③②①⑤④ |
| D、⑤②④①③ |
如果1g液氧中含有n个氧原子,则阿伏加德罗常数的值可表示为( )
A、
| ||
| B、n | ||
| C、16n | ||
| D、32n |
相同物质的量的 CO 和 CO2 相比较,下列叙述正确的是( )
①分子数之比为1:1
②所含氧原子数之比为1:2
③原子总数之比为2:3
④碳原子数之比为1:1
⑤电子数之比为7:11
⑥体积之比为1:1.
①分子数之比为1:1
②所含氧原子数之比为1:2
③原子总数之比为2:3
④碳原子数之比为1:1
⑤电子数之比为7:11
⑥体积之比为1:1.
| A、①③④ | B、②③④ |
| C、①②③④⑤ | D、①②③④⑤⑥ |
下列有关表述正确的是( )
A、次氯酸的电子式: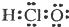 |
B、N原子的电子排布图: |
| C、二氧化硅的分子式:SiO2 |
| D、氯原子的价电子排布式:3s23p5 |