题目内容
已知氯水中存在如下的平衡:Cl2+H2O?HCl+HClO,欲使饱和氯水中的HClO的浓度增大,可在氯水中加入下列哪种物质( )
分析:反应Cl2+H2O?HCl+HClO达到平衡后,要使HClO浓度增加,应使平衡向正反应方向移动,HCl为强酸,HClO为弱酸,酸性比碳酸弱,以此解答该题.
解答:解:A.碳酸氢钠和HCl反应,平衡正向移动,能使HClO浓度增加,故A正确;
B.通入一些氯气,对于已经建立溶解平衡的体系来说,不会引起成分浓度的变化,故B错误;
C、加入HCl,溶液氢离子浓度增大,平衡向逆反应方向移动,HClO浓度减小,故C错误;
D、加入氢氧化钠颗粒,和盐酸次氯酸均反应,HClO浓度减小,故D错误;
故选A.
B.通入一些氯气,对于已经建立溶解平衡的体系来说,不会引起成分浓度的变化,故B错误;
C、加入HCl,溶液氢离子浓度增大,平衡向逆反应方向移动,HClO浓度减小,故C错误;
D、加入氢氧化钠颗粒,和盐酸次氯酸均反应,HClO浓度减小,故D错误;
故选A.
点评:本题考查化学平衡的影响,题目难度不大,本题易错点为D,注意加入水,溶液体积增大的倍数要大于HClO物质的量增大的倍数,HClO浓度降低.

练习册系列答案
相关题目
 KI3
KI3

 室温下,将Cl2缓慢通入水中.当通入的Cl2体积为V1时达到饱和(假设Cl2在水中只发生如下反应:Cl2+H2O=HCl+HClO,溶液中c(H+)变化入下图中的曲线a.已知Cl2的溶解度随温度的升高而迅速降低,下列叙述中正确的( )
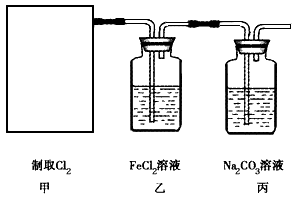
室温下,将Cl2缓慢通入水中.当通入的Cl2体积为V1时达到饱和(假设Cl2在水中只发生如下反应:Cl2+H2O=HCl+HClO,溶液中c(H+)变化入下图中的曲线a.已知Cl2的溶解度随温度的升高而迅速降低,下列叙述中正确的( ) 2CaSO4+2Cl2↑+2H2O。某学习小组利用此反应原理设计如图所示装置制取氯气并探究其性质。
2CaSO4+2Cl2↑+2H2O。某学习小组利用此反应原理设计如图所示装置制取氯气并探究其性质。