题目内容
A、B、C、D、E是五种短周期主族元素,它们的原子序数依次增大,其中A、D及B、E分别是同一主族元素,B、E两元素的原子核中质子数之和是A、D两元素原子核中质子数之和的2倍,则下列说法中正确的是( )
| A、与A形成化合物的稳定性C>B>E |
| B、形成简单离子的半径E>D>B |
| C、单质B和D在常温下化和生成D2B2 |
| D、C的最高价氧化物的水化物酸性最强 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:A、B、C、D、E是五种短周期主族元素,它们的原子序数依次增大,A、D及B、E分别是同一主族元素,确定B、E分别在二、三周期,由于B、E两元素的原子核中质子数之和是A、D两元素原子核中质子数之和的2倍,确定A、C在一、三周期,所以A为氢、D为钠,则B为氧、E为硫,结合原子序数可知C为F元素,据此解答.
解答:
解:A、B、C、D、E是五种短周期主族元素,它们的原子序数依次增大,A、D及B、E分别是同一主族元素,确定B、E分别在二、三周期,由于B、E两元素的原子核中质子数之和是A、D两元素原子核中质子数之和的2倍,确定A、C在一、三周期,所以A为氢、D为钠,则B为氧、E为硫,结合原子序数可知C为F元素,
A.非金属性C(F)>B(O)>E(S),则氢化物稳定性C(F)>B(O)>E(S),故A正确;
B.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越小,故离子半径E(S2-)>B(O2-)>D(Na+),故B错误;
C.钠与氧气在常温下反应生成氧化钠,故C错误;
D.C为F元素,没有最高价含氧酸,故D错误,
故选A.
A.非金属性C(F)>B(O)>E(S),则氢化物稳定性C(F)>B(O)>E(S),故A正确;
B.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越小,故离子半径E(S2-)>B(O2-)>D(Na+),故B错误;
C.钠与氧气在常温下反应生成氧化钠,故C错误;
D.C为F元素,没有最高价含氧酸,故D错误,
故选A.
点评:本题考查结构性质位置关系应用,推断元素是解题关键,注意理解分析A、D与B、E所处的周期,难度中等.

练习册系列答案
相关题目
下列关于硫及含硫化合物的叙述正确的是( )
| A、SO2的漂白原理与次氯酸相同 |
| B、硫在空气中燃烧生成大量SO3 |
| C、浓硫酸可以干燥H2、NH3、CO2等气体 |
| D、硫粉为黄色固体 |
间二甲苯苯环上的一个氢原子被-NO2取代后,其一元取代产物的同分异构体有( )
| A、1种 | B、2种 | C、3种 | D、4种 |
下列各有机物的命名中正确的是( )
| A、CH3-CH═CH-CH3 二丁烯 |
| B、CH3OOCC2H5 乙酸乙酯 |
C、 2-甲基-3-丁醇 2-甲基-3-丁醇 |
D、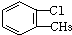 邻氯甲苯 邻氯甲苯 |
下列实验操作不正确的是( )
A、 倾倒液体 |
B、 检查气密性 |
C、 稀释浓硫酸 |
D、 取用固体 |
下列离子反应方程式正确的是( )
| A、次氯酸钙溶液中通入少量二氧化碳:Ca2++2ClO-+H2O+CO2═CaCO3↓+2H++2ClO- |
| B、澄清的石灰水跟盐酸反应:H++OH-=H2O |
| C、碳酸氢钠溶液中滴入氢氧化钙溶液:HCO3-+OH-═CO32-+H2O |
| D、硫化钡中加入足量稀硫酸:BaS+2H+═H2S↑+Ba2+ |
下列实验装置图及实验用品均正确的是(部分夹持仪器未画出)( )
A、 实验室用酒精制取乙烯 |
B、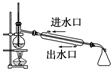 石油分馏 |
C、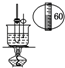 实验室制硝基苯 |
D、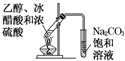 实验室制取乙酸乙酯 |
 钨是我国丰产元素.自然界中钨主要以钨(+6)酸盐的形式存在.黑钨矿的主要成分是铁和锰的钨酸盐(FeWO4、MnWO4).黑钨矿传统冶炼工艺流程图如图:
钨是我国丰产元素.自然界中钨主要以钨(+6)酸盐的形式存在.黑钨矿的主要成分是铁和锰的钨酸盐(FeWO4、MnWO4).黑钨矿传统冶炼工艺流程图如图: