题目内容
T℃时,CaCO3和CaF2的Ksp分别为1.0×10-10和4.0×10-12.下列说法正确的是( )
| A、T℃时,两饱和溶液中c(Ca2+ ):CaCO3>CaF2 |
| B、T℃时,两饱和溶液等体积混合,会析出CaF2固体 |
| C、T℃时,CaF2固体在稀盐酸中的Ksp比在纯水中的Ksp大 |
| D、T℃时,向CaCO3悬浊液中加NaF固体,可能析出CaF2固体 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:A、依据Ksp结合沉淀溶解平衡计算钙离子浓度减小;
B、依据钙离子浓度和碳酸根离子浓度计算浓度商和碳酸钙Ksp减小;
C、Ksp随温度变化,不随浓度变化;
D、沉淀的条件是溶液中离子的浓度商大于Ksp,会发生沉淀.
B、依据钙离子浓度和碳酸根离子浓度计算浓度商和碳酸钙Ksp减小;
C、Ksp随温度变化,不随浓度变化;
D、沉淀的条件是溶液中离子的浓度商大于Ksp,会发生沉淀.
解答:
解:A、T℃时,饱和CaCO3溶液中c(Ca2+)=c(CO32-)=
mol/L,饱和CaF2溶液c(Ca2+)?c(F-)2=4.0×10-12,c(Ca2+)=
mol/L;所以饱和CaCO3溶液和饱和CaF2溶液相比,后者的c(Ca2+)大于前者,故A错误;
B、等体积混合后的c(Ca2+)会较饱和CaCO3溶液中的c(Ca2+)大许多倍,c(Ca2+)=
mol/L+
×
(mol/L);
c(CO32-)只减少到原来的一半为
mol/L,此时溶液中的c(Ca2+)×c(CO32-)=(
mol/L+
×
mol/L)×
×
mol/L>Ksp(CaCO3)=1.0×10-10,所以会析出CaCO3固体,故B错误;
C、T℃时,CaCO3固体盐酸中的Ksp与在纯水中的Ksp相同,因沉淀的Ksp随温度变化,不随浓度改变,故C错误;
D、T℃时,在CaCO3悬浊液中加入NaF固体,当c(Ca2+)?c(F-)2≥Ksp(CaF2)时,CaCO3能转化为CaF2,故D正确;
故选:D.
| 1.0×10-10 |
| 3 | 4.0×10-12 |
B、等体积混合后的c(Ca2+)会较饱和CaCO3溶液中的c(Ca2+)大许多倍,c(Ca2+)=
| 1 |
| 2 |
| 1.0×10-10 |
| 1 |
| 2 |
| 3 | 1.0×10-12 |
c(CO32-)只减少到原来的一半为
| 1 |
| 2 |
| 1.0×10-10 |
| 1 |
| 2 |
| 1.0×10-10 |
| 1 |
| 2 |
| 3 | 1.0×10-12 |
| 1 |
| 2 |
| 1.0×10-10 |
C、T℃时,CaCO3固体盐酸中的Ksp与在纯水中的Ksp相同,因沉淀的Ksp随温度变化,不随浓度改变,故C错误;
D、T℃时,在CaCO3悬浊液中加入NaF固体,当c(Ca2+)?c(F-)2≥Ksp(CaF2)时,CaCO3能转化为CaF2,故D正确;
故选:D.
点评:本题考查了沉淀溶解平衡的应用,平衡的移动和沉淀生成的条件分析,溶度积常数的计算应用是解题关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
已知4种无机化合物在水中和液氨中的溶解度(g/100g溶剂)为:
由此溶解度可知在水溶液中上述化合物发生复分解反应为:2AgNO3+BaCl2=2AgCl↓+Ba(NO3)2,那么上述几种化合物在液氨溶液中发生复分解反应的化学方程式( )
| 物质 | AgNO3 | Ba(OH)2 | AgCl | BaCl2 |
| 水中 | 216 | 9.02 | 35.8 | |
| 液氨 | 86 | 97.2 | 0.8 | 0 |
| A、2AgNO3+BaCl2=2AgCl↓+Ba(NO3)2 |
| B、2AgNO3+BaCl2=2AgCl+Ba(NO3)2↓ |
| C、2AgCl+Ba(NO3)2=2AgNO3↓+BaCl2 |
| D、2AgCl+Ba(NO3)2=2AgNO3+BaCl2↓ |
下列关于Na2O与Na2O2的说法中,不正确的是( )
| A、Na2O2具有漂白性 |
| B、均与水反应生成NaOH,因而均是碱性氧化物 |
| C、Na2O中氧-2价,Na2O2中氧-1价 |
| D、均可与H2O、CO2反应 |
海洋中有丰富的食品、矿产、能源和药物.如图是从海水中提取某些原料的流程图.下列有关说法正确的是( )


| A、从海水中提取物质都必须通过化学反应才能实现 |
| B、第②步属于物理变化 |
| C、从第④~⑤步的目的是浓缩、富集溴单质 |
| D、第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入试剂的顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
将4mol A 气体和2mol B气体置于1L的密闭容器中,混合后发生如下反应:2A(g)+B(g)═2C(g),若经2s后测得C的浓度为1.2mol/L,下列说法正确的是( )
| A、用物质A表示的反应速率为1.2 mol/(L?s) |
| B、2 s时物质A的转化率为30% |
| C、用物质B表示的反应速率为0.6 mol/(L?s) |
| D、2 s时物质B的浓度为0.6 mol/L |
家用炒菜锅用水清洗后,出现红棕色的锈斑.在此变化过程中不发生的化学反应是( )
| A、4Fe(OH)2+2H2O+O2═4Fe(OH)3 |
| B、2Fe+2H2O+O2═2Fe(OH)2 |
| C、正极反应:2H2O+O2+4 e-→4OH- |
| D、负极反应:Fe→Fe3++3 e- |
下列各组离子能大量共存且溶液颜色为无色的是( )
| A、Na+、MnO4-、K+、NO3-、SO32- |
| B、Na+、CO32-、Cl-、Al3+、NO3- |
| C、Na+、S2-、OH-、K+、Cl-、NO3- |
| D、Fe2+、H+、Na+、Ca2+、NO3- |
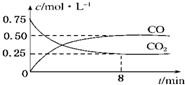 某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g),测得CO2和CO浓度随时间的变化如图所示:
某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g),测得CO2和CO浓度随时间的变化如图所示: