题目内容
11.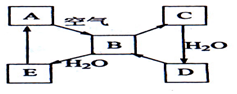 如图表示某淡黄色固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C含有的元素种类相同,且相对分子质量之比为4:5,化合物D是重要的工业原料.
如图表示某淡黄色固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C含有的元素种类相同,且相对分子质量之比为4:5,化合物D是重要的工业原料.(1)写出A在加热条件下与H2反应的化学方程式H2+S$\frac{\underline{\;\;△\;\;}}{\;}$H2S
(2)写出E与A的氢化物反应生成A的化学方程式H2SO3+2H2S═3S↓+3H2O
(3)写出一个由D与金属铜生成B的化学方程式Cu+2H2SO4 (浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(4)将足量的E溶液与NaOH溶液混合,写出反应的化学方程式H2SO3+NaOH=NaHSO3+H2O.
分析 A为淡黄色固体单质,应为S,由转化关系可知B为SO2,C为SO3,它们的相对分子质量为64:80=4:5,恰好与题意相符,则D为H2SO4,它是一种重要的工业原料,与题意也相符,SO2和水反应生成E为H2SO3,结合物质的性质以及题目要求可解答该题.
解答 解:(1)A为S,可与氢气反应生成硫化氢,反应的方程式为H2+S$\frac{\underline{\;\;△\;\;}}{\;}$H2S,故答案为:H2+S$\frac{\underline{\;\;△\;\;}}{\;}$H2S;
(2)H2SO3与H2S反应生成S,反应的方程式为H2SO3+2H2S═3S↓+3H2O,故答案为:H2SO3+2H2S═3S↓+3H2O;
(3)在加热条件下,铜和浓硫酸发生氧化还原反应生成硫酸铜、二氧化硫和水,反应方程式为Cu+2H2SO4 (浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4 (浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(4)足量的E溶液与NaOH溶液混合生成NaHSO3,方程式为H2SO3+NaOH=NaHSO3+H2O,故答案为:H2SO3+NaOH=NaHSO3+H2O.
点评 本题考查无机物的推断,为高频考点,侧重学生的分析能力的考查,注意淡黄色固体单质为该题的突破口进行推断,注意把握物质的化学性质,能熟练书写反应的化学方程式.

练习册系列答案
相关题目
2.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.2mol/LCaCl2溶液中含Cl-数为0.4NA | |
| B. | 标准状况下,1.12L H2S气体分子中含0.5NA个质子 | |
| C. | 常温常压下,23 g NO2和N2O4的混合气体一定含有NA个氧原子 | |
| D. | 标准状况下,4.48L的水中含有H2O分子的数目为0.2NA |
19.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=10-10的溶液:K+、Ba2+、NO3-、Cl- | |
| B. | 0.1mol/LNaAlO2溶液:H+、Na+、Cl-、SO42- | |
| C. | 与Al反应放出H2的溶液:Mg2+、Ca2+、HCO3-、NO3- | |
| D. | 中性溶液:Fe3+、K+、Cl-、SO42- |
6.下列有关阿伏加德罗常数(NA)的说法不正确的是( )
| A. | 12 g12C所含有的碳原子数为NA个 | |
| B. | NA的近似值为6.02×1023 | |
| C. | 2 mol H2O含有的H2O分子数目为2NA个 | |
| D. | 2NA个Cl2的质量为71 g |
16.下列离子方程式书写正确的是( )
| A. | Cu(OH)2中加入硫酸:OH-+H+=H2O | |
| B. | 钠加入水中:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 铁片与氯化铜溶液反应:Fe+Cu2+=Cu+Fe2+ | |
| D. | 向Ba(OH)2溶液中滴加稀硫酸:Ba2++OH-+H++SO42-=H2O+BaSO4↓ |
3.25℃时,下列溶液中各离子的浓度关系不正确的是( )
| A. | 等体积、等浓度的K2CO3溶液与盐酸混合,则混合液中:c(K+)>c(Cl-)>c(HCO3-)>c(OH-)>c(H+) | |
| B. | 向氨水中滴加盐酸至中性,则溶液中:c(NH4+)=c(Cl-)>c(OH-)=c(H+) | |
| C. | 等体积、等浓度的CH3COOH溶液与NaOH溶液混合后,溶液的pH=8,则c(OH-)-c(CH3COOH)=1×10-8mol•L-1 | |
| D. | 等体积、等浓度①NaCl、②CH3COONa、③NaClO溶液中离子总数大小顺序:③>②>① |
20.关于下列各装置图的叙述不正确的是( )
| A. | 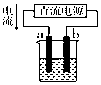 用装置精炼铜,则b极为精铜,电解质溶液为CuSO4溶液 | |
| B. | 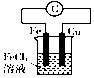 装置的总反应是Cu+2Fe3+=Cu2++2Fe2+ | |
| C. | 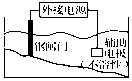 装置中钢闸门应与外接电源的负极相连 | |
| D. | 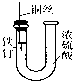 装置中的铁钉浸入浓硫酸中几乎没被腐蚀 |
