题目内容
下列说法正确的是( )
| A、检验氯乙烷中的氯元素时,将氯乙烷和NaOH溶液混合加热后,先用稀硫酸进行酸化,再加人AgN03溶液进行检验 |
| B、为了加快过滤速度以及得到较干燥的硅酸白色胶状沉淀可以采用抽滤的方法 |
| C、通常采用产生气泡的快慢,来比较不同条件下Na2S2O3溶液与稀硫酸的反应速率 |
| D、银氨溶液不能留存,久置后会变成氮化银,容易爆炸 |
考点:物质的检验和鉴别的基本方法选择及应用,物质的分离、提纯和除杂
专题:化学实验基本操作
分析:A.不能利用硫酸酸化,硫酸银为沉淀,干扰离子检验;
B.颗粒太小的沉淀易在滤纸上形成一层密实的沉淀,溶液不易透过;
C.应注意控制变量比较反应速率;
D.银氨溶液不稳定,易分解生成氮化银.
B.颗粒太小的沉淀易在滤纸上形成一层密实的沉淀,溶液不易透过;
C.应注意控制变量比较反应速率;
D.银氨溶液不稳定,易分解生成氮化银.
解答:
解:A.检验氯乙烷中的氯元素时,将氯乙烷和NaOH溶液混合加热后,先用稀硝酸进行酸化,再加人AgN03溶液进行检验,故A错误;
B.因胶状沉淀易穿透滤纸,颗粒太小的沉淀易在滤纸上形成一层密实的沉淀,溶液不易透过,则不能利用抽滤的方法加快反应速率,故B错误;
C.控制条件下,比较不同温度下产生气泡的快慢,来比较Na2S2O3溶液与稀硫酸的反应速率或相同温度下,改变硫酸的浓度观察气泡快慢比较反应速率,故C错误;
D.银氨溶液不稳定,久置后会变成氮化银,容易爆炸,所以不能留存,故D正确;
故选D.
B.因胶状沉淀易穿透滤纸,颗粒太小的沉淀易在滤纸上形成一层密实的沉淀,溶液不易透过,则不能利用抽滤的方法加快反应速率,故B错误;
C.控制条件下,比较不同温度下产生气泡的快慢,来比较Na2S2O3溶液与稀硫酸的反应速率或相同温度下,改变硫酸的浓度观察气泡快慢比较反应速率,故C错误;
D.银氨溶液不稳定,久置后会变成氮化银,容易爆炸,所以不能留存,故D正确;
故选D.
点评:本题考查物质检验和鉴别及混合物分离提纯等,为高频考点,涉及氯离子检验、反应速率比较及物质的性质等,选项B为解答的难点,C为解答的易错点,注意抽滤可加快颗粒较大的物质分离,比较反应速率应控制变量,题目难度中等.

练习册系列答案
相关题目
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、0.1mol/L的NaOH溶液:K+、AlO2-、SO42-、CO32- | ||
| B、0.1mol/LFeCl3溶液:K+、NH4+、I-、SCN- | ||
| C、0.1mol/L的Na2CO3溶液:K+、Ba2+、NO3-、Cl- | ||
D、
|
下列各离子浓度的比较,正确的是( )
| A、0.1mol?L-1 CH3COONa溶液中:c(OH-)>c(CH3COOH)+c(H+) |
| B、0.1mol?L-1的NH4Cl溶液与0.05mol?L-1的NaOH溶液等体积混合后溶液显碱性:c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+) |
| C、酸式盐NaHB在水溶液中,HB-的电离程度小于HB-的水解程度,则:c(Na+)>c(HB-)>c(OH-)>c(B2-)>c(H+) |
| D、1.0L 0.3mol?L-1 NaOH溶液缓慢通入CO2气体至溶液增重8.8g,所得溶液中:c(Na+)=c(HCO3-)+2c(CO32-)+c(OH-)-c(H+) |
下列说法正确的是( )
| A、苯酚钠溶液中通入CO2气体后产生白色沉淀,通过抽滤可分离出苯酚 |
| B、滴定实验时,锥形瓶用蒸馏水洗净后,直接盛待测液 |
| C、基于硫代硫酸钠与稀硫酸反应生成S和SO2,在定量测定反应速率时,既可用S对标记遮盖法,也可用排水法测SO2体积,计算出其的反应速率 |
| D、某溶液加入盐酸酸化的BaCl2溶液,若有白色沉淀生成,则原溶液含有SO42- |
下列叙述正确的是( )


| A、雌二醇和睾丸素两种物质的分子组成相差一个CH2,但不属于同系物 |
B、按系统命名法,有机物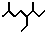 可命名为2,6-二甲基-4-乙基辛烷 可命名为2,6-二甲基-4-乙基辛烷 |
| C、氯气与甲烷在光照射的取代反应历程为:光照下,甲烷分子失去一个氢原子和甲基,甲基再与Cl2碰撞生成CH3Cl和氯自由基(Cl?) |
D、瘦肉精学名克伦特罗,结构如图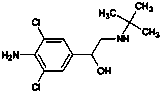 ,可以发生取代、加成、水解、酯化、消去反应 ,可以发生取代、加成、水解、酯化、消去反应 |
下列溶液中各离子的浓度关系不正确的是( )
| A、0.1mol?L-1 CH3COONa溶液中:c(CH3COO-)+c(CH3COOH)=0.1mol?L-1 |
| B、浓度均为0.1 mol?L-1 Na2CO3溶液和稀盐酸等体积混合后的溶液中:c(CO32-)+c(OH-)=c(H+)+c(H2CO3) |
| C、25℃时,pH=9.4、浓度均为0.1 mol?L-1的HCN与NaCN的混合溶液中:c(Na+)>c(CN-)>c(HCN)>c(OH-) |
| D、3.0L 0.1mol?L-1 NaOH溶液中缓慢通入CO2至溶液增重8.8 g时,溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
下列反应对应的离子方程式书写正确的是( )
| A、用氢氟酸在玻璃上“刻字”:SiO2+4H++4F-═SiF4↑+2H2O |
| B、实验室制取氯气:2MnO4-+8H++6Cl-═2MnO2↓+3Cl2↑+4H2O |
| C、将铁粉放入硫酸铁和硫酸铜的混合溶液中,初始阶段发生的反应:Fe+2Fe3+═3Fe2+ |
| D、常温下,铁与过量的浓硝酸反应:Fe+6H++3NO3-═Fe3++3NO2↑+3H2O |
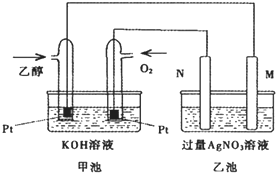 如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题: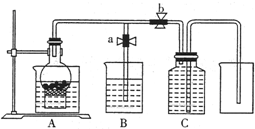 某同学设计如图所示装置来试验用粗铁粒与某浓度稀硝酸反应制取NO气体.
某同学设计如图所示装置来试验用粗铁粒与某浓度稀硝酸反应制取NO气体.