题目内容
19.下列物质中和苯互为同系物的是( )| A. | 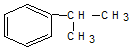 | B. | 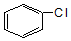 | C. | 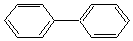 | D. | 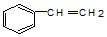 |
分析 结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物;互为同系物的物质满足以下特点:结构相似、化学性质相似、分子式通式相同、分子式不同、物理性质不同,研究对象是有机物,
苯的同系物是含一个苯环,在分子组成上相差一个或若干个CH2原子团的有机物为苯的同系物;
解答 解:A. 含一个苯环,在分子组成上相差两个CH2原子团,是苯的同系物,故A正确;
含一个苯环,在分子组成上相差两个CH2原子团,是苯的同系物,故A正确;
B. 分子中含氯原子,属于卤代烃,不是苯的同系物,故B错误;
分子中含氯原子,属于卤代烃,不是苯的同系物,故B错误;
C. 分子中含两个苯环,和苯结构不相似,不是苯的同系物,故C错误;
分子中含两个苯环,和苯结构不相似,不是苯的同系物,故C错误;
D.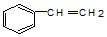 分子中含碳碳双键,和苯结构不相似,不是苯的同系物,故D错误;
分子中含碳碳双键,和苯结构不相似,不是苯的同系物,故D错误;
故选A.
点评 本题考查了苯的同系物的判断,题目难度不大,注意掌握常见有机物的分类、同系物的概念及判断方法,掌握基础是解题关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.W、X、Y、Z四中短周期主族元素的原子序数依次增大,它们的K层电子数总和为7,L层电子数总和为20,M层电子数总和为7,且W与Y同主族.下列说法正确的是( )
| A. | 单质的还原性:W>Y | |
| B. | 最高价氧化物对应的水化物的酸性:X>Z | |
| C. | W的阳离子和Z的阴离子均能促进水的电离 | |
| D. | 由W、Y、Z三种元素组成的化合物既含离子键又含共价键 |
14.煤、石油、天然气是人类使用的主要能源,下列说法正确的是( )
| A. | 煤、石油、天然气均为混合物,煤中含有苯等有机物 | |
| B. | 石油裂化和煤的干馏都是化学变化,而石油的分馏和煤的气化都是物理变化 | |
| C. | 石油的裂解主要目的是提高汽油的产量和质量 | |
| D. | 汽油燃烧产生的汽车尾气中,所含的大气污染物主要是碳氮的氧化物 |
4.从防止污染和减少用酸量的角度分析,下列制取Cu(NO3)2的方法中最好的是( )
| A. | Cu$\stackrel{浓硝酸}{→}$Cu(NO3)2 | |
| B. | Cu$\stackrel{稀硝酸}{→}$Cu(NO3)2 | |
| C. | Cu$→_{△}^{O_{2}}$CuO$\stackrel{硝酸}{→}$Cu(NO3)2 | |
| D. | Cu$→_{△}^{浓硫酸}$CuSO4$\stackrel{Ba(NO_{3})_{2}}{→}$Cu(NO3)2 |
11.某化学小组对Na2SO3和AgNO3在不同pH下的反应及产物,进行了以下实验探究.
查阅资料:Ⅰ.Ag2SO3:白色、难溶于水;
Ⅱ.Ag2O:棕黑色、难溶于水,易与酸溶液反应.
(1)根据资料:
①通常情况Na2SO3溶液和AgNO3溶液反应产生的现象是产生白色浑浊.
②若Ag2O与盐酸反应,其化学方程式应为Ag2O+2HCl=2AgCl+H2O.
(2)检测溶液pH:
①0.1mol/LAgNO3溶液的pH=5,引发这一结果的微粒是Ag+.
②0.1mol/LNa2SO3溶液的pH=10,其原因用离子方程式解释是SO32-+H2O=HSO3-+OH-.
(3)实验探究:在不同pH条件下Na2SO3溶液与AgNO3溶液混合反应.实验记录如图:
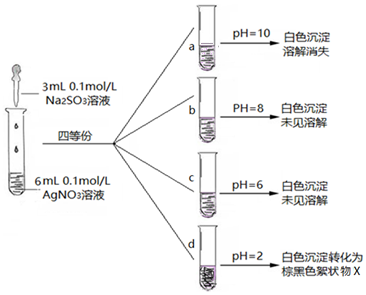
Ⅰ.实验a中沉淀溶解消失的原因,可能是Ag2SO3在碱性较强条件下,溶解或Ag2SO3被氧化成Ag2SO4溶解.
Ⅱ.Ag2SO3在溶液中沉淀析出的大致pH范围是6-8.
Ⅲ.将d中棕黑色絮状物X滤出、洗净、进行实验分析:
①由实验ⅰ得出的结论是黑棕色沉淀不是Ag2O.
②d中的棕黑色絮状物X是Ag.
③实验ⅱ中的化学反应方程式是Ag+2HNO3(浓)=AgNO3+NO2↑+H2O.
(4)小组认为在酸性条件下,SO32-的还原性增强,生成X的化学方程式是Ag2SO3+H2O=2Ag+H2SO4.
查阅资料:Ⅰ.Ag2SO3:白色、难溶于水;
Ⅱ.Ag2O:棕黑色、难溶于水,易与酸溶液反应.
(1)根据资料:
①通常情况Na2SO3溶液和AgNO3溶液反应产生的现象是产生白色浑浊.
②若Ag2O与盐酸反应,其化学方程式应为Ag2O+2HCl=2AgCl+H2O.
(2)检测溶液pH:
①0.1mol/LAgNO3溶液的pH=5,引发这一结果的微粒是Ag+.
②0.1mol/LNa2SO3溶液的pH=10,其原因用离子方程式解释是SO32-+H2O=HSO3-+OH-.
(3)实验探究:在不同pH条件下Na2SO3溶液与AgNO3溶液混合反应.实验记录如图:

Ⅰ.实验a中沉淀溶解消失的原因,可能是Ag2SO3在碱性较强条件下,溶解或Ag2SO3被氧化成Ag2SO4溶解.
Ⅱ.Ag2SO3在溶液中沉淀析出的大致pH范围是6-8.
Ⅲ.将d中棕黑色絮状物X滤出、洗净、进行实验分析:
| 实验 | 操作 | 现象 |
| ⅰ | 将其置于试管中加稀盐酸、观察 | 无明显现象 |
| ⅱ | 将其置于试管中加足量浓硝酸、观察 | 立即产生红棕色气体 |
| ⅲ | 在ⅱ反应所得溶液中,加Ba(NO3)2溶液、观察,再加BaCl2、观察 | 前者无明显现象,后者出现白色沉淀 |
②d中的棕黑色絮状物X是Ag.
③实验ⅱ中的化学反应方程式是Ag+2HNO3(浓)=AgNO3+NO2↑+H2O.
(4)小组认为在酸性条件下,SO32-的还原性增强,生成X的化学方程式是Ag2SO3+H2O=2Ag+H2SO4.
1.某同学在实验室中发现了一瓶无色而有刺激性气味的气体,根据气味判断可能是氨气,但不能确定是氨气.下列提供的方法中,能帮他检验该气体是否为氨气的是( )
| A. | 将湿润的红色石蕊试纸放在打开的瓶口 | |
| B. | 将湿润的蓝色石蕊试纸放在打开的瓶口 | |
| C. | 用蘸有浓硫酸的玻璃棒靠近打开的瓶口. | |
| D. | 将干燥的红色石蕊试纸放在瓶口 |
 表中表示的一些物质或概念间的从属关系中不正确的是( )
表中表示的一些物质或概念间的从属关系中不正确的是( )