题目内容
工业上可用CO2生产甲醇,反应为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。将6mol CO2和8 mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。图中虚线表示仅改变某一反应条件时,H2物质的量随时间的变化。下列说法正确的是
CH3OH(g)+H2O(g)。将6mol CO2和8 mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。图中虚线表示仅改变某一反应条件时,H2物质的量随时间的变化。下列说法正确的是
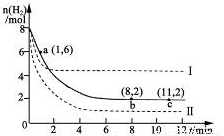
A.反应开始至a点时v(H2)=1mol·L-1·min-1
B.若曲线I对应的条件改变是升高温度,则该反应△H>0
C.曲线II对应的条件改变是降低压强
D.保持温度不变,若将平衡后的容器体积缩小至1L,重新达平衡时则2 mol·L-1<c(CH3OH) <8/3 mol·L-1
【答案】
AD
【解析】CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
反应开始至a点时H22mol,v(H2)=1mol·L-1·min-1,A正确。升高温度速率加快,平衡向逆向运动,逆向吸热,正向放热,B错误。曲线II对应的条件改变是时间变短,加快速率,平衡正移,增加压强,C错误。保持温度不变,若将平衡后的容器体积缩小至1L,相当于加压,向正向移动,重新达平衡时则2 mol·L-1<c(CH3OH) <8/3 mol·L-1。

练习册系列答案
相关题目
 工业上可用CO2生产甲醇,反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).将6molCO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示.图中虚线表示仅改变某一反应条件时,H2物质的量随时间的变化.下列说法正确的是( )
工业上可用CO2生产甲醇,反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).将6molCO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示.图中虚线表示仅改变某一反应条件时,H2物质的量随时间的变化.下列说法正确的是( )| A、反应开始至a点时v(H2)=1mol?L-1?min-1 | B、若曲线I对应的条件改变是升高温度,则该反应△H>0 | C、曲线II对应的条件改变是降低压强 | D、保持温度不变,若将平衡后的容器体积缩小至1L,重新达平衡时则2 mol?L-1<c(CH3OH)<8/3 mol?L-1 |
 工业上可用CO2生产甲醇,反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).将6mol CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示.图中虚线表示仅改变某一反应条件时,H2物质的量随时间的变化.请回答下列问题:
工业上可用CO2生产甲醇,反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).将6mol CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示.图中虚线表示仅改变某一反应条件时,H2物质的量随时间的变化.请回答下列问题: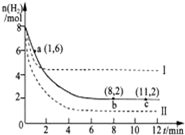 工业上可用CO2生产甲醇,反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).将6mol CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示.图中虚线表示仅改变某一反应条件时,H2物质的量随时间的变化.下列说法正确的是( )
工业上可用CO2生产甲醇,反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).将6mol CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示.图中虚线表示仅改变某一反应条件时,H2物质的量随时间的变化.下列说法正确的是( )