题目内容
将湿润的淀粉KI试纸伸入盛入Cl2的集气瓶中,有何现象?并设计实验验证反应的机理.
答案:
解析:
提示:
解析:
|
先变蓝后褪色 设计实验如下:
溶液褪色是因为单质碘被过量氯气所氧化生成无色的HIO3 |
提示:
|
思路点拨:许多同学都答出了先变蓝后褪色,但在回答褪色理由究竟是Cl2和水作用生成的HClO有漂白作用,还是单质碘被过量氯气所氧化,这涉及到Cl2的强氧化性,不仅能将I-氧化为I2,还能将I2氧化为HIO3. 2KI+Cl2 5Cl2+I2+6H2O 小结点评:化学是一门以实验为基础的科学,化学实验题可以考查学生的实验能力和创造能力,所以实验题有很好的区分和选拔功能,而答好实验题的关键就是同学们必须亲自动手做实验,积累实验知识,锻炼提高实验技能,并对实验中出现的现象深入思考. |

练习册系列答案
相关题目

 (1)原电池反应通常是放热反应,下列化学反应在理论上可设计成原电池是
(1)原电池反应通常是放热反应,下列化学反应在理论上可设计成原电池是
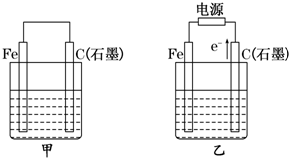 如图甲、乙是电化学实验装置.
如图甲、乙是电化学实验装置.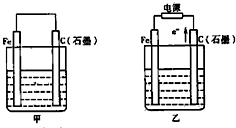 如图甲、乙是电化学实验装置.
如图甲、乙是电化学实验装置.