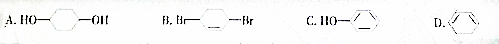题目内容
4.下列物质中,既能发生消去反应,又能氧化成醛的是( )| A. | 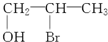 | B. | 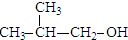 | C. | 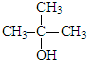 | D. | 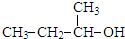 |
分析 醇发生消去反应的结构特点是:与羟基所连碳相邻的碳上有氢原子才能发生消去反应,形成不饱和键;醇发生氧化反应的结构特点是:有羟基所连碳上有氢原子的才能发生氧化反应.卤代烃发生消去反应的结构特点是:只有-X相连碳相邻碳上有氢原子的才能发生消去反应,形成不饱和键,以此解答该题、
解答 解:A.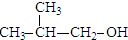 含有-CH2OH,可被氧化生成醛,羟基邻位含有H原子,可发生消去反应,故A正确;
含有-CH2OH,可被氧化生成醛,羟基邻位含有H原子,可发生消去反应,故A正确;
B.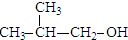 含有-CH2OH,可被氧化生成醛,羟基邻位含有H原子,可发生消去反应,故B正确;
含有-CH2OH,可被氧化生成醛,羟基邻位含有H原子,可发生消去反应,故B正确;
C.不能发生催化氧化,故C错误;
D.可发生催化氧化,但生成酮,故D错误.
故选AB.
点评 本题考查即有机物的结构和性质,侧重考查醇的消去反应、氧化反应,以及卤代烃的消去反应 难度不大,注意醇发生消去反应的结构特点是:只有羟基相连碳的相邻碳上有氢原子的才能发生消去反应,形成不饱和键;醇发生氧化反应的结构特点是:只有羟基相连碳的碳上有氢原子的才能发生氧化反应.

练习册系列答案
相关题目
15.若pH=2的酸溶液和pH=12的碱溶液等体积混合后溶液呈碱性,其原因可能( )
| A. | 反应后盐水解使溶液呈碱性 | B. | 弱酸溶液和强碱溶液反应 | ||
| C. | 强酸溶液和弱碱溶液反应 | D. | 一元强酸溶液和一元强碱溶液反应 |
12.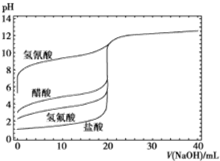 如图是用0.1mol/LNaOH溶液分别滴定20mL浓度均为0.1mol/L的不同一元酸的滴定曲线,下列说法错误的是( )
如图是用0.1mol/LNaOH溶液分别滴定20mL浓度均为0.1mol/L的不同一元酸的滴定曲线,下列说法错误的是( )
 如图是用0.1mol/LNaOH溶液分别滴定20mL浓度均为0.1mol/L的不同一元酸的滴定曲线,下列说法错误的是( )
如图是用0.1mol/LNaOH溶液分别滴定20mL浓度均为0.1mol/L的不同一元酸的滴定曲线,下列说法错误的是( )| A. | 酸性:HF>CH3COOH>HCN | |
| B. | 用NaOH溶液滴定醋酸时,应用酚酞做指示剂不能使用甲基橙 | |
| C. | 当加入10mLNaOH溶液时,c(CN-)>c(CH3COO-) | |
| D. | 随NaOH溶液的滴入,CH3COOH溶液中水的电离程度先变大后变小 |
19.二氧化碳的捕集、利用与封存是能源领域的一个重要研究课题
(1)在太阳能作用下,以CO2为原料制取碳(C)的流程如图1所示.
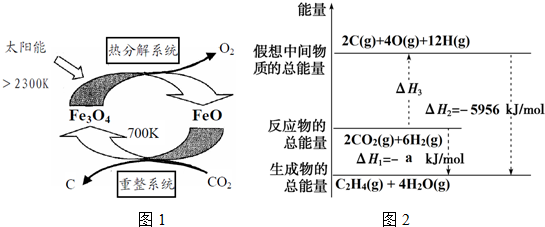
①热分解系统每分解0.5mol Fe3O4转移电子的物质的量为1mol.
②该系统的总反应的化学方程式是CO2═C+O2.
(2)二氧化碳催化加氢可合成低碳烯:
2CO2(g)+6H2(g)?C2H4(g)+4H2O(g)△H1=-a kJ•mol-1,有关能量变化如图2所示:
①几种物质具有的能量(在标准状况下,规定单质的能量为0,测得其他物质在生成时放出或吸收的热量即为其具有的能量)如表所示:
则a=128
②几种化学键的键能如下:
则b=436
(3)据报道以二氧化碳为原料采用特殊的电极电解强酸性的二氧化碳水溶液可得到多种燃料,其原理如图三所示.
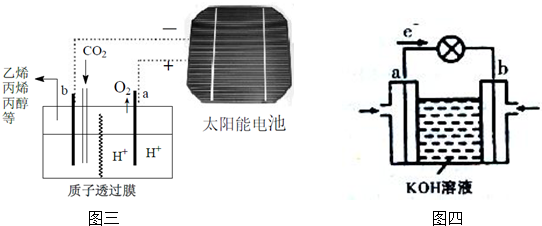
①该工艺中能量转化方式主要有太阳能转化为电能、电能转化为化学能(写出其中两种形式即可).
②其中b极上生成丙烯(CH3CH=CH2)的电极反应式为3CO2+18H++18e-=CH3CH=CH2+6H2O.
③乙烯和氧气反应通过上图四装置可将化学能转化为电能,b电极反应式为O2+2H2O+4e-=4OH-.
(1)在太阳能作用下,以CO2为原料制取碳(C)的流程如图1所示.

①热分解系统每分解0.5mol Fe3O4转移电子的物质的量为1mol.
②该系统的总反应的化学方程式是CO2═C+O2.
(2)二氧化碳催化加氢可合成低碳烯:
2CO2(g)+6H2(g)?C2H4(g)+4H2O(g)△H1=-a kJ•mol-1,有关能量变化如图2所示:
①几种物质具有的能量(在标准状况下,规定单质的能量为0,测得其他物质在生成时放出或吸收的热量即为其具有的能量)如表所示:
| 物质 | CO2(g) | C2H4(g) | H2O(g) |
| 能量/kJ•mol-1 | -394 | 52 | -242 |
②几种化学键的键能如下:
| 化学键 | C=O | H-H | C=C | O-H |
| 键能/kJ•mol-1 | 803 | b | 615 | 463 |
(3)据报道以二氧化碳为原料采用特殊的电极电解强酸性的二氧化碳水溶液可得到多种燃料,其原理如图三所示.

①该工艺中能量转化方式主要有太阳能转化为电能、电能转化为化学能(写出其中两种形式即可).
②其中b极上生成丙烯(CH3CH=CH2)的电极反应式为3CO2+18H++18e-=CH3CH=CH2+6H2O.
③乙烯和氧气反应通过上图四装置可将化学能转化为电能,b电极反应式为O2+2H2O+4e-=4OH-.
9.如果1g水中含有n个氢原子,则阿伏加德罗常数是( )
| A. | $\frac{1}{n}$ mol-1 | B. | 9n mol-1 | C. | 2nmol-1 | D. | 18nmol-1 |
16.下列表示式错误的是( )
| A. | Al3+的结构示意图: | B. | 氯化钠的电子式: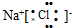 | ||
| C. | 铝离子的电子式:Al3+ | D. | 铝原子的结构示意图: |
14.下列关于反应能量的说法正确的是( )
| A. | Zn(s)+CuSO4(aq)═ZnSO4(aq)+Cu(s)△H<0,反应物总能量>生成物总能量 | |
| B. | 相同条件下1 mol氢原子所具有的能量为E1,1 mol 氢分子所具有的能量为E2,则2E1=E2 | |
| C. | 101 kPa时,2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1,则H2的燃烧热为571.6 kJ•mol-1 | |
| D. | H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,则1 mol NaOH的氢氧化钠固体与含0.5 mol H2SO4的稀硫酸混合后放出57.3 kJ的热量 |
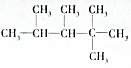 的烷烃,则此烯烃可能的结构简式是CH2=CHCH3CHCH3C(CH3)3、(CH3)2C=CCH3C(CH3)3、(CH3)2CHC=CH2C(CH3)3.
的烷烃,则此烯烃可能的结构简式是CH2=CHCH3CHCH3C(CH3)3、(CH3)2C=CCH3C(CH3)3、(CH3)2CHC=CH2C(CH3)3.