题目内容
18.某学习小组的同学对氯气与铁的反应及产物进行了如下探究,已知FeCl3在100℃左右时升华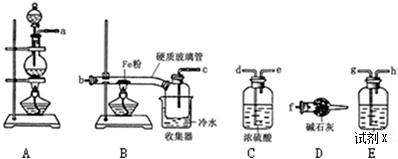
(1)装置的连接顺序为a→g→h→d→e→b→c→f
(2)装置D的作用吸收过量氯气;试剂X为饱和食盐水.
(3)硬质玻璃管与收集器之间没有用导管连接,原因是防止堵塞.
(4)B中的反应开始前,需排除装置中的空气,应采取的方法是A中的反应进行一段时间后,看到共绿色气体充满装置,再开始加热B.
(5)将所得FeCl3固体溶于水,则该溶液呈酸性(填“中性”、“酸性”或“碱性”)
分析 实验室用浓盐酸与二氧化锰加热制备氯气,浓盐酸易挥发,制备的氯气中含有氯化氢和水,依次通过盛有饱和食盐水、浓硫酸的洗气瓶除去氯化氢和水蒸气,得到纯净干燥的氯气,铁在氯气中燃烧生成氯化铁.
(1)排列顺序为气体的制取→洗气→干燥→氯气和铁的反应→尾气处理;
(2)浓盐酸易挥发,制备的氯气中含有氯化氢,依据氯化氢与氯气在饱和食盐水中溶解度不同,选择饱和食盐水除杂;氯气有毒,能与碱反应,可以用碱石灰吸收过量的氯气;
(3)Fe在氯气中燃烧生成棕褐色烟,导气管口较细,易堵塞;
(4)利用生成的氯气排出装置中的空气来分析;
(5)氯化铁为强酸弱碱盐,溶于水,三价铁离子水解生成氢氧化铁和氯化氢;
解答 解:(1)实验室用浓盐酸与二氧化锰加热制备氯气,浓盐酸易挥发,制备的氯气中含有氯化氢和水,浓硫酸具有吸水性能作氯气干燥剂、碱石灰具有碱性而吸收氯气、饱和食盐水吸收氯化氢而抑制氯气溶解,装置排列顺序为气体的制取→洗气→干燥→氯气和铁的反应→尾气处理,所以装置连接顺序为a→g→h→d→e→b→c→f,
故答案为:g;h;d;e;
(2)浓盐酸易挥发,制备的氯气中含有氯化氢,氯化氢易溶液水,而氯气在饱和食盐水中溶解度很小,所以选择饱和食盐水除去氯气中的氯化氢;氯气有毒,能与碱反应,可以用碱石灰吸收过量的氯气;
故答案为:故答案为:吸收过量的氯气;饱和食盐水;
(3)Fe在氯气中燃烧生成棕褐色烟,棕褐色烟冷却易生成固体,导气管口较细,易堵塞,所以硬质玻璃管与收集器之间没有用导管连接,
故答案为:防止堵塞;
(4)B中的反应开始前,需排除装置中的空气,防止氧气和铁反应生成铁的氧化物而产生杂质,所以B中的反应开始前,必须排除装置中的空气,其方法是A中的反应进行一段时间后,看到共绿色气体充满装置,再开始加热B,
故答案为:A中的反应进行一段时间后,看到共绿色气体充满装置,再开始加热B;
(5)氯化铁为强酸弱碱盐,溶于水,三价铁离子水解生成氢氧化铁和氯化氢,溶液显酸性;
故答案为:酸性.
点评 本题考查了制备实验方案中的有关知识,难度不大,明确氯气制备原理及性质是解题关键,侧重考查学生对基础知识的应用能力.

| A. | 将铁粉加到稀硝酸中 | |
| B. | 向稀盐酸中滴入少量的NaAlO2溶液 | |
| C. | 向MgSO4、H2SO4的混合溶液中加入过量的Ba(OH)2溶液 | |
| D. | 室温下,NaOH溶液与醋酸溶液反应后所得的pH大于7的溶液 |
| A. | S | B. | Mg | C. | P | D. | Cl |
| A. | 硝酸银溶液 | B. | 浓硫酸 | C. | 纯碱溶液 | D. | 碱石灰 |
| A. | 烧杯 | B. | 量筒 | C. | 试管 | D. | 酒精灯 |
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放
入25.00mL待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL.
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.试回答下列问题:
(1)锥形瓶中的溶液从红色变为无 色时,停止滴定.
(2)滴定时边滴边摇动锥形瓶,眼睛应观察B
A、滴定管内液面的变化 B、锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是待测溶液润洗锥形瓶由此造成的测定结果偏高(偏高、偏低或无影响)
(4)步骤②缺少的操作是据酸式滴定管用蒸馏水洗净后,应用标准液润洗
(5)如图,是某次滴定时的滴定管中的液面,其读数为22.60mL
(6)
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前度数(mL) | 滴定后度数(mL) | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 4.00 | 24.10 |
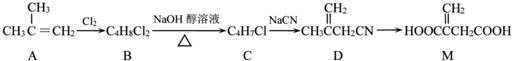
 +NaOH$→_{△}^{乙醇}$
+NaOH$→_{△}^{乙醇}$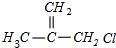 +NaCl+H2O,其反应类型为消去反应.
+NaCl+H2O,其反应类型为消去反应.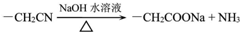 ,D经五步转成变成M的合成反应流程为:
,D经五步转成变成M的合成反应流程为: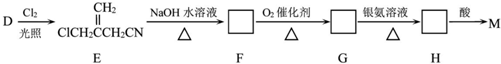
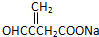 ;
;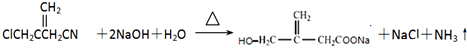 ;
;