题目内容
影响化学反应速率的因素很多.在下列事实中,影响反应速率的外界条件分别为:
(1)夏天的食品易霉变,冬天不易发生该现象 ;
(2)在5%的H2O2溶液中加入1滴~2滴1mol∕LFeCl3溶液,很快产生气体 ;
(3)工业上常将固体燃料粉碎,以提高燃烧效率 .
(1)夏天的食品易霉变,冬天不易发生该现象
(2)在5%的H2O2溶液中加入1滴~2滴1mol∕LFeCl3溶液,很快产生气体
(3)工业上常将固体燃料粉碎,以提高燃烧效率
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:常见影响反应速率的因素有浓度、温度、压强、催化剂等,一般来说,浓度越大、温度越高、压强越大,反应速率越大,加入催化剂,可增大反应速率,以此解答该题.
解答:
解:(1)在夏天温度高,反应速率快,食品易霉变,冬天温度低,反应速率慢,不易发生该现象,故答案为:温度;
(2)在5%的H2O2溶液中加入1滴~2滴1mol∕LFeCl3溶液,FeCl3是催化剂,可以加快反应速率,故答案为:催化剂;
(3)工业上常将固体燃料粉碎,是为了加大固体的表面积,加快化学反应速率,故答案为:固体表面积.
(2)在5%的H2O2溶液中加入1滴~2滴1mol∕LFeCl3溶液,FeCl3是催化剂,可以加快反应速率,故答案为:催化剂;
(3)工业上常将固体燃料粉碎,是为了加大固体的表面积,加快化学反应速率,故答案为:固体表面积.
点评:本题考查影响化学反应速率的影响,为高频考点,把握内因及常见的外因为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
关于下列各装置图的叙述中,正确的是( )
A、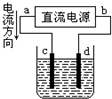 d极发生氧化反应、c极发生还原反应 |
B、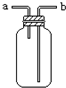 从a口通入气体,可用于收集H2、NH3、NO等气体 |
C、 X若为CCl4,上层为稀硫酸,可用于吸收氨气,并防止倒吸 |
D、 可用于干燥、收集氯化氢,并吸收多余的氯化氢 |
25℃、101kPa下:①2NaOH(s)+CO2(g)═Na2CO3(s)+H2O(l)△H=a kJ/mol ②NaOH(s)+CO2(g)═NaHCO3(s)△H=b kJ/mol,下列说法正确的是( )
| A、25℃、101kPa下:2NaHCO3(s)═Na2CO3(s)+H2O(l)+CO2(g)△H=(2b-a) kJ/mol |
| B、相同温度下,同物质的量浓度的碳酸钠和碳酸氢钠溶液中的离子种类相同 |
| C、相同温度、压强条件下,向等体积等物质的量浓度的碳酸钠和碳酸氢钠中加入足量的盐酸,产生的二氧化碳不相等 |
| D、碳酸钠固体和碳酸氢钠固体中阴阳离子个数比相同 |
0.5mol氧气的质量是( )
| A、8g | B、16g |
| C、24g | D、32g |
已知:电离平衡常数:H2SO3>H2CO3>HClO>HCO3- (25℃),氧化性:KMnO4>Cl2>Br2>Fe3+.下列离子方程式正确的是( )
| A、FeBr2溶液中滴加少量氯水:2Br-+Cl2═Br2+2Cl- |
| B、NaClO溶液中通入少量CO2:2ClO-+CO2+H2O═2HClO+CO32- |
| C、浓盐酸中加入KMnO4:2KMnO4-+10Cl-+16H+═2Mn2++5Cl2↑+8H2O |
| D、足量SO2通入NaHCO3溶液中:2HCO3-+SO2═SO32-+2CO2+H2O |
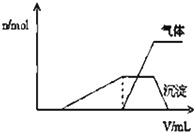 1L某混合溶液中可能含有的离子如下表:
1L某混合溶液中可能含有的离子如下表: