题目内容
18.已知短周期元素的离子aA3+、bB+、cC2-、dD- 都具有相同的电子层结构,判断下列关系正确的是( )| A. | 原子序数:a>b>d>c | B. | 原子半径:A>B>C>D | ||
| C. | 离子的还原性:D->C2- | D. | 气态氢化物的稳定性:H2C>HD |
分析 短周期元素的离子:aA3+、bB+、cC2-、dD-都具有相同的电子层结构,则核外电子数相等,所以有:a-3=b-1=c+2=d+1,C、D为非金属,应处于第二周期,A、B为金属应处于第三周期,结合离子所带电荷,可知C为O元素,D为F元素,A为Al元素,B为Na元素,结合元素周期律解答.
解答 解:短周期元素的离子:aA3+、bB+、cC2-、dD-都具有相同的电子层结构,则核外电子数相等,所以有:a-3=b-1=c+2=d+1,C、D为非金属,应处于第二周期,A、B为金属应处于第三周期,结合离子所带电荷,可知C为O元素,D为F元素,A为Al元素,B为Na元素.
A.核外电子数相等,所以有:a-3=b-1=c+2=d+1,则原子序数a>b>d>c,故A正确;
B.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径:B>A>C>D,故B错误;
C.同周期随原子序数增大非金属性增强,故非金属性O<F,则离子还原性:O2->F-,故C错误;
D.非金属性O<F,非金属性越强氢化物越稳定,故氢化物稳定性:HF>H2O,故D错误.
故选A.
点评 本题考查结构与位置关系、元素周期律等,难度中等,注意元素周期律的理解掌握,也可以根据电荷与核外电子排布相同推断元素在周期表中的位置而不需要推断具体的元素.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.质量相同的下列有机物,在足量氧气中完全燃烧时,消耗氧气物质的量最多的是( )
| A. | 苯 | B. | 甲烷 | C. | 乙烯 | D. | 乙醇 |
6.下列关于有机物的性质或应用说法不正确的是( )
| A. | 苯和油脂均不能使酸性KMnO4褪色 | |
| B. | CH2Cl2只有一种结构说明甲烷分子是正四面体结构,而不是平面正方形结构 | |
| C. | 蒸馏和分馏都是通过沸点不同分离液态混合物的 | |
| D. | 油脂皂化反应的产物是高级脂肪酸和甘油 |
13.如图是部分短周期元素原子半径与原子序数的关系图.则下列说法正确的是( )
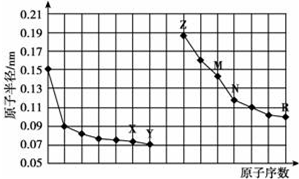

| A. | 简单离子的半径:X<Z<M | |
| B. | 最高价氧化物对应水化物的酸性:R<N | |
| C. | Y、R两种元素的气态氢化物稳定性:Y>R | |
| D. | 由X与N两种元素组成的化合物不能与任何酸反应,但能与强碱反应 |
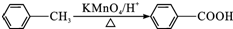
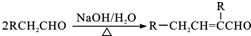
 .
. .
.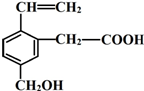 某有机物的结构简式如图,该物质不应有的化学性质是⑥⑦
某有机物的结构简式如图,该物质不应有的化学性质是⑥⑦