��Ŀ����
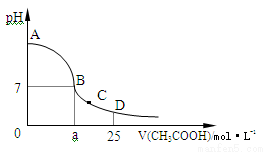
������һ��ǿ�ᣬŨ�ȳ���40��ʱ�ᷢ���ֽ⣬��Ӧ�ɱ�ʾΪ�� a HClO3 = bO2��+ c Cl2��+ d HClO4 + e H2O�������й�˵������ȷ����
A���ɷ�Ӧ��ȷ����������HClO3��O2
B��������ֽ����û������lmol�����������Ϊ45g����Ӧ����ʽ�ɱ�ʾΪ��3HClO3 = 2O2��+ C12��+ HClO4 + H2O
C���ɷǽ�����Cl��S������֪����HClO3��H2SO4
D������ѧ������a=8��b=3����÷�Ӧת�Ƶ�����Ϊ20e��
C
��������
���������A����������ԭ��Ӧ�У������ԣ�������>������������ڸ÷�Ӧ����������HClO3������������O2������������HClO3��O2����ȷ��B.n(O2)��n(C12)=2:1ʱ�������ƽ��Ħ�������ǣ�2��32+71��-45g/mol�����Դ�ʱ�ֽⷴӦ�ķ���ʽ�ǣ�3HClO3 = 2O2��+ C12��+ HClO4 + H2O����ȷ��C��Ԫ�صķǽ�����Խǿ��������������Ӧ��ˮ��������Ծ�Խǿ������Ԫ�صķǽ�����Cl��S�����Կ���֪����HClO4��H2SO4������D������ѧ������a=8��b=3����÷�Ӧ����ʽ�ǣ�8HClO3 = 3O2��+ 2C12��+ 4HClO4 + 2H2O�����ݷ���ʽ��֪��ÿ��8mol��HClO3������Ӧ��ת�Ƶ��ӵ����ʵ�����20NA����ÿ8��HClO3������Ӧ��ת�Ƶ�������20e������ȷ��
���㣺����������ԭ��Ӧ�����ʵ������ԵıȽϡ�����ʽ����ƽ���������ԱȽϼ�����ת�Ƶ�֪ʶ��

 �ʰ�Ӣ��ͬ����ϰ��ϵ�д�
�ʰ�Ӣ��ͬ����ϰ��ϵ�д� ѧϰʵ����ϵ�д�
ѧϰʵ����ϵ�д� CaSiO3��CO2���ķ�����˵�����������ǿ��̼��
CaSiO3��CO2���ķ�����˵�����������ǿ��̼�� LiNH2+LiH��H2�������������ǻ�ԭ��
LiNH2+LiH��H2�������������ǻ�ԭ��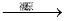 NO����Ũ����
NO����Ũ���� NO2��֪��������HNO3��ϡ��>Ũ����
NO2��֪��������HNO3��ϡ��>Ũ����
 Cr2O72-(��ɫ) +H2O
Cr2O72-(��ɫ) +H2O