题目内容
16.常温下将0.01mol NH4Cl和0.002mol NaOH溶于水配成1L溶液(1)该溶液中除H2O的电离平衡外还存在的平衡体系是水解平衡,NH4++H2O?NH3•H2O+H+,电离平衡,NH3•H2O?NH4++OH-.
(2)溶液中共有7种不同的微粒.
(3)这些粒子中浓度为0.01mol•L-1的是Cl-,浓度为0.002mol•L-1的是Na+.
(4)物质的量之和为0.01mol的两种微粒是NH4+、NH3•H2O.
分析 常温下将0.01mol NH4Cl和0.002mol NaOH溶于水配成1L溶液,氯化铵和氢氧化钠反应生成一水合氨和氯化钠,反应的定量关系可知氯化铵过量,溶液中为NH3•H2O、NaCl、NH4Cl溶质,依据化学方程式计算判断溶液中的溶质微粒,结合电荷守恒计算判断问题;
(1)氯化铵和氢氧化钠反应生成一水合氨和氯化钠,氯化铵过量,溶液中存在铵根离子水解平衡,一水合氨形成的化学平衡,水的电离平衡;
(2)依据溶液中平衡状态和存在的微粒分析,溶液中为NH3•H2O、NaCl、NH4Cl溶质和溶剂水,一水合氨电离出铵根离子和氢氧根离子,氯化钠完全电离出钠离子和氯离子,氯化铵电离出铵根离子和氯离子,水电离出氢离子和氢氧根离子;
(3)钠离子、氯离子在溶液中不发生变化,这些微粒中浓度为0.01mol/L的是Cl-,浓度为0.002mol/L的是Na+;
(4)依据物料守恒分析,氮元素守恒,溶液中氮元素的存在形式为一水合氨和铵根离子,物质的量之和为0.01mol的两种微粒是NH4+、NH3•H2O.
解答 解:常温下将0.01mol NH4Cl和0.002mol NaOH溶于水配成1L溶液,氯化铵和氢氧化钠反应生成一水合氨和氯化钠,氯化铵过量,溶液中为NH3•H2O、NaCl、NH4Cl溶质,
(1)氯化铵和氢氧化钠反应生成一水合氨和氯化钠,氯化铵过量,溶液中存在铵根离子水解平衡,NH4++H2O?NH3•H2O+H+,一水合氨是弱电解质存在电离平衡,NH3•H2O?NH4++OH-,溶液中溶剂水也是弱电解质存在电离平衡,H2O?OH-+H+,该溶液中除H2O的电离平衡外还存在的平衡体系是水解平衡,NH4++H2O?NH3•H2O+H+,一水合氨的电离平衡,NH3•H2O?NH4++OH-,
故答案为:水解平衡,NH4++H2O?NH3•H2O+H+,电离平衡,NH3•H2O?NH4++OH-;
(2)溶液中为NH3•H2O、NaCl、NH4Cl溶质和溶剂水,溶液中存在的微粒为NH4+、OH-、H+、Na+、Cl-、NH3•H2O、H2O,共7种微粒;
故答案为:7;
(3)这些微粒中,铵根离子水解,一水合氨发生电离,改变了溶液中铵根离子浓度、一水合氨浓度、氢离子浓度和氢氧根离子浓度,而氯离子、钠离子物质的量不变,所以浓度为0.01mol/L的是Cl-,浓度为0.002mol/L的是Na+;
故答案为:Cl-;Na+;
(4)物料守恒分析,0.01mol NH4Cl溶于0.002mol NaOH溶于水配成1L溶液,铵根离子结合氢氧根离子生成一水合氨,一水合氨电离书写铵根离子和氢氧根离子,根据物料守恒可知,氮元素的存在形式为NH4+、NH3•H2O,但溶液中存在的氮元素物质的量一定为1mol,则物质的量之和为0.01mol的两种微粒是NH4+、NH3•H2O;
故答案为:NH4+、NH3•H2O.
点评 本题考查了弱电解质电离,盐类水解原理,明确影响平衡移动的因素、电解质溶液中电荷守恒、物料守恒,掌握基础是关键,题目难度中等.

| A. | n+4 | B. | n+6 | C. | n+8 | D. | n+10 |
| A. | N2H4+O2═N2+2H2O△H=-534.4 kJ•mol-1 | |
| B. | N2H4+O2═N2+2H2O△H=-1 068.8 kJ•mol-1 | |
| C. | N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534.4 kJ•mol-1 | |
| D. | $\frac{1}{2}$N2H4(g)+$\frac{1}{2}$O2(g)═$\frac{1}{2}$N2(g)+H2O(g)△H=+267.2 kJ•mol-1 |
| A. | 48gO3含有的氧原子数目为NA | |
| B. | 常温常压下,22.4L Cl2含有的分子数目为NA | |
| C. | 1molAl与足量氢氧化钠溶液完全反应时失去的电子数目为3NA | |
| D. | 1mol•L-1K2CO3溶液中含有的钾离子数目为2NA |
| A. | 稀豆浆 | B. | NaCl溶液 | C. | Fe(OH)3胶体 | D. | H2SiO3胶体 |
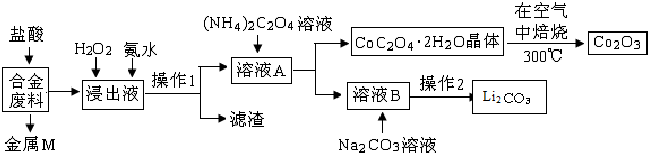
已知:Ksp[Cu(OH)2]=4.0×10-21,Ksp[Al(OH)3]=1.0×10-32,Ksp[Fe(OH)3]=1.0×10-38,Ksp[Fe(OH)2]=8.0×10-19.pH=7.3时Li+或Co3+开始沉淀.
(1)金属M为Cu.
(2)①加入H2O2的作用是(用离子方程式表示)2Fe2++H2O2+2H+=2Fe3++2H2O.
②氨水的作用是调节溶液的pH,室温下,使溶液中杂质离子刚好沉淀完全而全部除去(浓度小于1.0×10-5mol•L-1).需调节溶液pH范围为5.0<pH<7.3.
(3)充分焙烧的化学方程式为4CoC2O4?2H2O+3O2$\frac{\underline{\;焙烧\;}}{\;}$2Co2O3+8 H2O+8CO2.
(4)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见下表.操作2中,蒸发浓缩后必须趁热过滤,其原因是减少Li2CO3的溶解损失.
| 温度/℃ | 10 | 30 | 60 | 90 |
| 浓度/mol?L-1 | 0.21 | 0.17 | 0.14 | 0.10 |
(6)①用Li、Co形成某锂离子电池的正极是LiCoO2,含Li+导电固体为电解质.充电时,Li+还原为Li,并以原子形式嵌入电池负极材料碳-6(C6)中(如图a).电池反应为LixC6+Li1-xCoO2$?_{充电}^{放电}$C6+LiCoO2,
写出该电池放电时的负极反应式LixC6-xe-=C6+xLi+.
②锂硫电池的总反应为:2Li+S$?_{充电}^{放电}$Li2S,图b表示用锂离子电池给锂硫电池充电,请在图b的电极
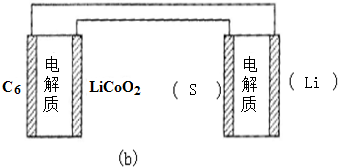 中填写“Li”或“S”,以达到给锂硫电池充电的目的.
中填写“Li”或“S”,以达到给锂硫电池充电的目的.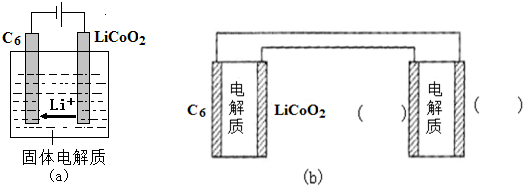
| A. | 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 | |
| B. | 开始蒸馏时,应该先通冷凝水,再加热;蒸馏完毕,应该先撤酒精灯再停通冷凝水 | |
| C. | 使用托盘天平称量物质时,先取小砝码,再依次取较大的砝码 | |
| D. | Ba(NO3)2溶于水,可将含有Ba(NO3)2的废液倒入水槽中,再用水冲入下水道 |
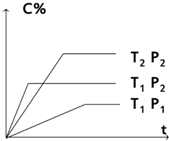 对于反应mA (g)+nB (g)?pC(g) 有如图所示的关系,
对于反应mA (g)+nB (g)?pC(g) 有如图所示的关系,