题目内容
 元素周期表揭示了化学元素间的内在联系,使其构成了一个完整的体系.
元素周期表揭示了化学元素间的内在联系,使其构成了一个完整的体系.(1)第二周期元素碳、氮、氧的电负性从大到小顺序为
(2)第四周期元素砷、硒、溴的第一电离能从大到小顺序为
(3)第ⅢA族元素原子具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质.
①[B(OH)4]-中B的原子杂化类型为
②不考虑空间构型,[B(OH)4]-的结构可用示意图表示为
(4)过渡区元素铜的离子是人体内多种酶的辅因子.某化合物Y 与Cu(Ⅰ)(Ⅰ表示化合价为+1)结合形成图1所示的离子:
①写出Cu(Ⅰ)的电子排布式
②该离子中含有化学键的类型有
A.极性键 B.离子键C.非极性键D.配位键
③向氯化铜溶液中通入足量的二氧化硫,生成白色沉淀M,M的晶胞结构如图2所示.写出该反应的离子方程式
考点:元素周期表的结构及其应用,位置结构性质的相互关系应用,配合物的成键情况,原子轨道杂化方式及杂化类型判断
专题:元素周期律与元素周期表专题
分析:(1)同周期从左向右第一电离能增大,但N原子p轨道半满,为稳定结构,则第一电离能更大;
(2)同周期从左向右第一电离能增大,但As原子p轨道半满,为稳定结构,则第一电离能比Se的大;
(3)[B(OH)4]-中B原子形成3个θ键,1个配位键,共含有4个价层电子对,所以采用sp3杂化;
(4)①根据能量最低原理和洪特规则书写电子排布式;
②同种非金属元素之间存在非极性键,不同非金属元素之间存在极性键,含有孤电子对的原子和含有空轨道的原子间存在配位键;
③利用均摊法确定M的化学式,铜离子和二氧化硫能发生氧化还原反应生成亚铜离子和硫酸根离子.
先计算一个CuCl分子的质量,再用均摊法求出一个晶胞含有的阴阳离子数,然后根据V=
求出其体积.
(2)同周期从左向右第一电离能增大,但As原子p轨道半满,为稳定结构,则第一电离能比Se的大;
(3)[B(OH)4]-中B原子形成3个θ键,1个配位键,共含有4个价层电子对,所以采用sp3杂化;
(4)①根据能量最低原理和洪特规则书写电子排布式;
②同种非金属元素之间存在非极性键,不同非金属元素之间存在极性键,含有孤电子对的原子和含有空轨道的原子间存在配位键;
③利用均摊法确定M的化学式,铜离子和二氧化硫能发生氧化还原反应生成亚铜离子和硫酸根离子.
先计算一个CuCl分子的质量,再用均摊法求出一个晶胞含有的阴阳离子数,然后根据V=
| m |
| ρ |
解答:
解:(1)同周期从左向右第一电离能增大,但N原子p轨道半满,为稳定结构,则第一电离能更大,所以第一电离能为C<O<N,故答案为:N>C>O;
(2)同周期从左向右第一电离能增大,但As原子p轨道半满,为稳定结构,则第一电离能比Se的大,所以第一电离能为Br>As>Se,故答案为:Br>As>Se;
(3)[B(OH)4]-中B原子形成3个θ键,1个配位键,共含有4个价层电子对,所以采用sp3杂化,结构可用示意图表示为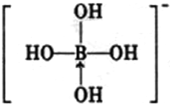 ,
,
故答案为:sp3; ;
;
(4)①Cu的电子排布式为1s22s22p63s23p63d104s1,失去一个电子后生成Cu+,其电子排布式为1s22s22p63s23p63d10,
故答案为:1s22s22p63s23p63d10;
②该离子中,氮原子和氮原子之间、碳原子和碳原子之间都存在非极性键,碳原子和氮原子之间、氮原子和氢原子之间、碳原子和氢原子之间都存在极性键,铜原子和氮原子间存在配位键;
故答案为:ACD;
③根据晶胞结构知,白色小球个数=8×
+6×
=4,黑色小球个数=4,所以该化合物的化学式为:CuCl,二氧化硫有还原性,铜离子有氧化性,所以二氧化硫和氯化铜发生氧化还原反应生成氯化亚铜和硫酸,离子反应方程式为:2Cu2++2Cl-+SO2+2H2O=2CuCl↓+SO42-+4H+.
1个“CuCl”的质量为
g,而用均摊法算出一个晶胞含有1个“CuCl”,即一个晶胞质量为
g,又有v=
=
=
cm3.
故答案为:2Cu2++2Cl-+SO2+2H2O=2CuCl↓+SO42-+4H+;
cm3.
(2)同周期从左向右第一电离能增大,但As原子p轨道半满,为稳定结构,则第一电离能比Se的大,所以第一电离能为Br>As>Se,故答案为:Br>As>Se;
(3)[B(OH)4]-中B原子形成3个θ键,1个配位键,共含有4个价层电子对,所以采用sp3杂化,结构可用示意图表示为
 ,
,故答案为:sp3;
 ;
;(4)①Cu的电子排布式为1s22s22p63s23p63d104s1,失去一个电子后生成Cu+,其电子排布式为1s22s22p63s23p63d10,
故答案为:1s22s22p63s23p63d10;
②该离子中,氮原子和氮原子之间、碳原子和碳原子之间都存在非极性键,碳原子和氮原子之间、氮原子和氢原子之间、碳原子和氢原子之间都存在极性键,铜原子和氮原子间存在配位键;
故答案为:ACD;
③根据晶胞结构知,白色小球个数=8×
| 1 |
| 8 |
| 1 |
| 2 |
1个“CuCl”的质量为
| 99g/mol |
| NA/mol |
| 99 |
| NA |
| m |
| ρ |
| ||
| ag/cm3 |
| 99 |
| NA |
故答案为:2Cu2++2Cl-+SO2+2H2O=2CuCl↓+SO42-+4H+;
| 99 |
| NA |
点评:本题考查晶体结构、杂化轨道、空间构型等,难度中等,主要考查学生阅读对题目信息与结构图获取知识的能力.

练习册系列答案
相关题目
下列化学用语正确的是( )
A、聚丙烯的结构简式: |
B、丙烷分子的比例模型: |
C、四氯化碳分子的电子式: |
| D、甲烷结构简式为CH4 |
 科学研究表明,月球上可能存在少量水:月岩中含有钛铁矿,其主要成分的晶胞如图所示.
科学研究表明,月球上可能存在少量水:月岩中含有钛铁矿,其主要成分的晶胞如图所示. 有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示.电池正极的电极反应式是
有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示.电池正极的电极反应式是