题目内容
17.海水是一个巨大的化学资源库,有关海水综合利用的说法正确的是( )| A. | 海水中含有钾元素,只需经过物理变化就可以得到钾单质 | |
| B. | 海水蒸发制海盐的过程中发生了化学变化 | |
| C. | 利用潮汐发电是将化学能转化为电能 | |
| D. | 从海水中可以得到NaCl,电解熔融NaCl可制备金属钠 |
分析 A.化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,海水中含有的钾元素是以K+的形式存在,生成钾单质有新物质生成;
B.海水中含有氯化钠,经过海水蒸发制得氯化钠,只发生了物理变化;
C.根据能量转化的方式分析,潮汐发电的原理是潮汐能转化为电能;
D.根据电解熔融氯化钠的原理分析.
解答 解:A.海水中含有的钾元素是以K+的形式存在,要转化为钾单质,钾元素必然降价,要发生还原反应,即只经过物理变化不能从海水中得到钾单质,故A错误;
B.海水中含有氯化钠,经过海水蒸发制得氯化钠,是溶液中溶质和溶剂的分离,只发生了物理变化,没有发生化学变化,故B错误;
C.利用朝汐发电是朝汐能转化为电能,没有发生化学反应,而化学能转化为电能必须要发生化学反应,故C错误;
D.从海水中得到氯化钠后,可以电解熔融状态的氯化钠2NaCl$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑,生成氯气和金属钠,故D正确;
故选D.
点评 本题考查化学变化、海水制盐原理、潮汐发电等,题目难度不大,注意海水蒸发制海盐的过程中的物理变化,主要考查基本知识和基本反应原理,需要正确记忆并深化理解.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
8.室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是( )
| A. | 溶液中导电粒子的数目增加,导电性增强 | |
| B. | 醋酸的电离程度增大,[H+]减小 | |
| C. | 电离平衡向右移动,电离常数Ka减少 | |
| D. | 稀释后溶液中由水电离出的[H+]=1×10-11 mol/L |
12. 常温下,向盛有1L0.1mol•L-1NaHSO4溶液的烧杯中不断滴加0.05mol/L的Ba(OH)2溶液,溶液中产生沉淀物质的量n(mol)与溶液pH的变化情况如图所示,下列说法不正确的是( )
常温下,向盛有1L0.1mol•L-1NaHSO4溶液的烧杯中不断滴加0.05mol/L的Ba(OH)2溶液,溶液中产生沉淀物质的量n(mol)与溶液pH的变化情况如图所示,下列说法不正确的是( )
 常温下,向盛有1L0.1mol•L-1NaHSO4溶液的烧杯中不断滴加0.05mol/L的Ba(OH)2溶液,溶液中产生沉淀物质的量n(mol)与溶液pH的变化情况如图所示,下列说法不正确的是( )
常温下,向盛有1L0.1mol•L-1NaHSO4溶液的烧杯中不断滴加0.05mol/L的Ba(OH)2溶液,溶液中产生沉淀物质的量n(mol)与溶液pH的变化情况如图所示,下列说法不正确的是( )| A. | A点时pH=1 | |
| B. | 恰好完全沉淀时Ba(OH)2溶液的体积为2L | |
| C. | B点时,溶液中的离子浓度关系为c(Na+)>c(SO42-)>c(H+)=c(OH-) | |
| D. | C点时pH=14 |
2.一份100ml 0.2mol/L的NaCl溶液,下列哪个选项与该溶液中的Cl-浓度相同( )
| A. | 200ml 0.1mol/LFeCl3溶液 | B. | 100ml 0.1mol/L MgCl2溶液 | ||
| C. | 200ml 0.1mol/L NaCl溶液 | D. | 100ml 0.4mol/L BaCl2溶液 |
7.某硫酸和硝酸的混合溶液20mL,其中含有硫酸的浓度为2mol•L-1,含有硝酸的浓度为1mol•L-1,现向其中加入0.96g 铜粉,充分反应后(假设只生成NO气体),最多可收集到标准状况下的气体的体积为( )
| A. | 224 mL | B. | 168 mL | C. | 112 mL | D. | 448 mL |
 Ⅰ.尿素在农业生产中起重要作用,其合成过程分两步进行:
Ⅰ.尿素在农业生产中起重要作用,其合成过程分两步进行: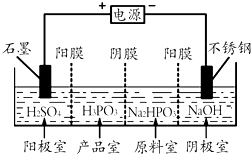 亚磷酸(H3PO3)是二元酸,H3PO3溶液存在电离平衡:H3PO3?H++H2PO3-.亚磷酸与足量NaOH溶液反应,生成水和Na2HPO3.
亚磷酸(H3PO3)是二元酸,H3PO3溶液存在电离平衡:H3PO3?H++H2PO3-.亚磷酸与足量NaOH溶液反应,生成水和Na2HPO3.