题目内容
12.将如图所示实验装置的K闭合,下列判断正确的是( )
| A. | Cu 电极上发生氧化反应 | B. | 电子沿 Zn→a→b→Cu 路径流动 | ||
| C. | 片刻后可观察到滤纸a点变红色 | D. | 片刻后甲池中c(SO42-)增大 |
分析 甲、乙装置能自发的进行氧化还原反应,所以是原电池,锌易失电子作负极,铜作正极,则含有硫酸钠溶液的滤纸是电解池,a是阴极,b是阳极,阴极上氢离子放电,阳极上氢氧根离子放电,电子从负极沿导线流向电解池阴极,原电池放电时,阴离子向负极移动,阳离子向正极移动,据此分析.
解答 解:A.Zn作原电池的负极,Cu作原电池的正极,Cu电极是发生还原反应,故A错误;
B、电子流向是负极到正极,但a→b这一环节是在溶液中导电,是离子导电,电子并没沿此路径流动,故B错误;
C、滤纸处是电解池,a做阴极,氢离子放电,水电离平衡破坏附近氢氧根离子浓度增大,酚酞变红,故C正确;
D、甲池中锌离子浓度增大,盐桥中的氯离子移向甲池,硫酸根离子浓度基本不变,故D错误;
故选C.
点评 本题考查电化学知识,原电池、电解池原理的应用,装置图设计有些复杂,B选项干扰作用明显,设问巧妙,题目难度中等.

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
15.下列说法不正确的是( )
| A. | 石灰石-石膏法可用于燃煤的脱硫 | |
| B. | 钠和钾的合金在常温下是液体,可用于快中子反应堆作热交换剂 | |
| C. | 焦炭在炼铁高炉中用于提供热能和产生还原性气体CO | |
| D. | 氢氧化铁胶体可用于杀菌消毒 |
3.下列说法正确的是( )
| A. | 纤维素、乙酸乙酯、油脂和蛋白质在一定条件,都能水解 | |
| B. | 淀粉和纤维素互为同分异构体,化学式均为(C6H10O5)n | |
| C. | 羊毛、蚕丝、棉花和麻等天然高分子材料的主要成分都是蛋白质 | |
| D. | 淀粉、纤维素、蛋白质和油脂均属于天然高分子化合物 |
20.下列表示式错误的是( )
| A. | Na+的结构示意图: | B. | Na的电子排布式:1s22s22p63s1 | ||
| C. | Na+的轨道表示式: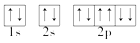 | D. | Na的简化电子排布式:[Ne]3s1 |
7.关于[Cr(H2O)4Cl2]Cl的说法正确的是( )
| A. | 中心原子的化合价为+2价 | |
| B. | 配体为水分子,外界为Cl- | |
| C. | 配位数是6 | |
| D. | 在其水溶液中加入AgNO3溶液,不产生白色沉淀 |
17.请按要求回答下列问题:
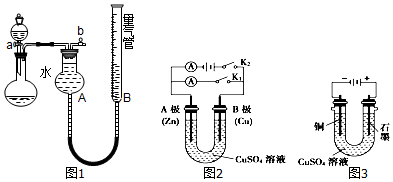
(1)某同学设计图1装置进行探究“铜和稀硝酸反应制取NO”的实验(夹持装置已略去),则制取NO的化学方程式为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O;
利用该装置还可制取并收集少量其他气体,请完成下表:
(2)根据图2回答:
①打开K1,合上K2.则此时此装置为电解池;
②A电极可观察到的现象是附着红色固体.
(3)根据图3回答:将纯净的CuSO4溶液放入如图所示的装置中进行电解,石墨电极上的电极反应式为4OH--4e-═2H2O+O2↑.图2对应的实验完成后,铜电极增重6.4g,石墨电极产生标准状况下的气体体积1.12L.

(1)某同学设计图1装置进行探究“铜和稀硝酸反应制取NO”的实验(夹持装置已略去),则制取NO的化学方程式为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O;
利用该装置还可制取并收集少量其他气体,请完成下表:
| 制取气体 | 药品 |
| O2 | H2O2、MnO2 |
| H2 | 某溶液NaOH(或HCl)、Al |
①打开K1,合上K2.则此时此装置为电解池;
②A电极可观察到的现象是附着红色固体.
(3)根据图3回答:将纯净的CuSO4溶液放入如图所示的装置中进行电解,石墨电极上的电极反应式为4OH--4e-═2H2O+O2↑.图2对应的实验完成后,铜电极增重6.4g,石墨电极产生标准状况下的气体体积1.12L.
4.下列物质长期露置于空气中会变质,但不是发生氧化还原反应的是( )
| A. | Na | B. | NaOH | C. | FeSO4 | D. | 氯水 |
10.有三种环烃结构如下
萘: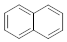 联苯:
联苯: 盆烯:
盆烯:
有关说法正确的是( )
萘:
 联苯:
联苯: 盆烯:
盆烯:
有关说法正确的是( )
| A. | 三种物质均难溶于水且均能使酸性高锰酸钾溶液褪色 | |
| B. | 一氯代物数目相同的是联苯和盆烯 | |
| C. | 盆烯是苯的同分异构体,联苯是苯的同系物 | |
| D. | 三种分子的碳原子均可能在同一平面内 |
11.下列物质中只含离子键的是( )
| A. | SO2 | B. | Na2O2 | C. | H2O2 | D. | NaC1 |