题目内容
下列微粒:①H3O+②NH4+③CH3COO-④NH3⑤CH4中含有配位键的是( )
| A、①② | B、①③ | C、④⑤ | D、②④ |
考点:配合物的成键情况
专题:化学键与晶体结构
分析:在物质或离子中中心原子含有空轨道,和含有孤电子对的原子或离子能形成配位键.
①H3O+中氢离子提供空轨道,氧原子提供孤电子对;
②NH4+氢离子提供空轨道,氮原子提供孤电子对;
③CH3COO- 中碳和氧最外层有8个电子达到稳定结构,氢满足2电子稳定结构,无空轨道,无孤电子对;
④氨气分子中氮原子含有孤电子对,但氢原子不含空轨道;
⑤CH4 分子中,碳原子与4个氢原子分别共用一对电子,形成4个C-H键,无空轨道,无孤电子对.
①H3O+中氢离子提供空轨道,氧原子提供孤电子对;
②NH4+氢离子提供空轨道,氮原子提供孤电子对;
③CH3COO- 中碳和氧最外层有8个电子达到稳定结构,氢满足2电子稳定结构,无空轨道,无孤电子对;
④氨气分子中氮原子含有孤电子对,但氢原子不含空轨道;
⑤CH4 分子中,碳原子与4个氢原子分别共用一对电子,形成4个C-H键,无空轨道,无孤电子对.
解答:
解:①H3O+中O提供孤电子对,H+提供空轨道,二者形成配位键,H3O+含有配位键;
②氨气分子中氮原子含有孤电子对,氢离子提供空轨道,可以形成配位键,NH4+含有配位键;
③CH3COO- 中碳和氧最外层有8个电子达到稳定结构,氢满足2电子稳定结构,无空轨道,无孤电子对,电子式为: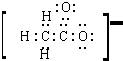 ,不含有配位键;
,不含有配位键;
④氨气的电子式为 ,氨气分子中氮原子含有孤电子对,但氢原子不含空轨道,所以不能形成配位键;
,氨气分子中氮原子含有孤电子对,但氢原子不含空轨道,所以不能形成配位键;
⑤甲烷中碳原子满足8电子稳定结构,氢原子满足2电子稳定结构,电子式为 ,无空轨道,无孤电子对,CH4不含有配位键;
,无空轨道,无孤电子对,CH4不含有配位键;
故选A.
②氨气分子中氮原子含有孤电子对,氢离子提供空轨道,可以形成配位键,NH4+含有配位键;
③CH3COO- 中碳和氧最外层有8个电子达到稳定结构,氢满足2电子稳定结构,无空轨道,无孤电子对,电子式为:
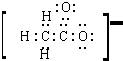 ,不含有配位键;
,不含有配位键;④氨气的电子式为
 ,氨气分子中氮原子含有孤电子对,但氢原子不含空轨道,所以不能形成配位键;
,氨气分子中氮原子含有孤电子对,但氢原子不含空轨道,所以不能形成配位键;⑤甲烷中碳原子满足8电子稳定结构,氢原子满足2电子稳定结构,电子式为
 ,无空轨道,无孤电子对,CH4不含有配位键;
,无空轨道,无孤电子对,CH4不含有配位键;故选A.
点评:本题考查配位键的形成条件及其应用等,题目难度中等,需要学生全面掌握配位键的形成条件,并能运用分析解决问题,注意配位键形成的条件,一方要提供空轨道,另一方提供孤电子对.

练习册系列答案
相关题目
联苯(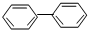 )由两个苯环通过单键连接而成,假定二氯联苯分子中,苯环间的单键可以自由旋转,理论上由异构而形成的二氯联苯共有( )
)由两个苯环通过单键连接而成,假定二氯联苯分子中,苯环间的单键可以自由旋转,理论上由异构而形成的二氯联苯共有( )
 )由两个苯环通过单键连接而成,假定二氯联苯分子中,苯环间的单键可以自由旋转,理论上由异构而形成的二氯联苯共有( )
)由两个苯环通过单键连接而成,假定二氯联苯分子中,苯环间的单键可以自由旋转,理论上由异构而形成的二氯联苯共有( )| A、6种 | B、9种 |
| C、10种 | D、12种 |
某温度下向100g澄清的饱和石灰水中加入5.6g生石灰,充分反应后恢复到原来的温度.下列叙述正确的是( )
| A、恢复到原温度后,溶液的浓度增大 |
| B、沉淀物的质量为7.4g |
| C、饱和石灰水的质量大于98.2g |
| D、恢复到原温度后,溶液的质量分数不变 |
俗话说“雷雨发庄稼”.在雷雨天,空气中有O3(由O2生成)和NO产生,下列说法正确的是( )
| A、O3和O2两种气体都是氧元素形成的单质,化学性质相同 |
| B、生成O3和NO的反应都是氧化还原反应 |
| C、NO在空气中不能稳定存在,会继续反应 |
| D、NO的产生是形成酸雨的主要原因 |
下列混合物可用加热的方法分离的是( )
| A、碘和氯化铵 |
| B、碳酸氢钠和二氧化锰 |
| C、硫酸钾和氯酸钾 |
| D、氯化铵和氯化钡 |
NO2被水吸收的反应中,发生氧化反应的物质与发生还原反应的物质的质量比为( )
| A、1:2 | B、2:1 |
| C、1:3 | D、3:1 |
用铜作催化剂,使1-丙醇氧化为某有机物,下列物质中,与该有机物互为同分异构体的是( )
| A、CH3OCH2CH3 |
| B、CH3CH(OH)CH3 |
| C、CH3COCH3 |
| D、CH3COOCH3 |
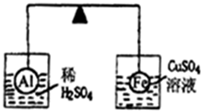 在杠杆的两端分别挂着质量、体积都相同的铝球和铁球,此时杠杆平衡.然后将两球分别浸没在稀硫酸和硫酸铜溶液中片刻,如图所示,则下列说法正确的是( )
在杠杆的两端分别挂着质量、体积都相同的铝球和铁球,此时杠杆平衡.然后将两球分别浸没在稀硫酸和硫酸铜溶液中片刻,如图所示,则下列说法正确的是( )| A、铝球一定是空心的 |
| B、左边烧杯中的溶液质量减少了 |
| C、去掉两烧杯杠杆仍平衡 |
| D、右边铁球上出现红色 |