题目内容
能正确表示下列反应的离子方程式为( )
A、用铁棒作阴极、炭棒作阳极电解饱和氯化钠溶液:2Cl-+2H2O
| ||||
| B、NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O | ||||
| C、将1mol/L NaAlO2溶液和1.5mol/L的HCl溶液等体积互相均匀混合:3AlO2-+6H+=2 Al(OH)3↓+Al3+ | ||||
| D、NaClO溶液与FeCl2溶液混合:Fe2++2ClO-+2H2O=Fe(OH)2↓+2HClO |
考点:离子方程式的书写
专题:离子反应专题
分析:A.用铁棒作阴极、炭棒作阳极电解饱和氯化钠溶液,反应生成氢氧化钠、氢气、氯气;
B.漏掉氨根离子与氢氧根离子的反应;
C.1molNaAIO2 先与1molHCI反应生成1molAI(OH)3,还剩0.5molHCI与1/6molAI(OH)3反应生成
molAlCl3和
molH20,两个方程式相加,就得到总方程式;
D.次氯酸根具有强的氧化性能够氧化二价铁离子.
B.漏掉氨根离子与氢氧根离子的反应;
C.1molNaAIO2 先与1molHCI反应生成1molAI(OH)3,还剩0.5molHCI与1/6molAI(OH)3反应生成
| 1 |
| 6 |
| 1 |
| 2 |
D.次氯酸根具有强的氧化性能够氧化二价铁离子.
解答:
解:A.用铁棒作阴极、炭棒作阳极电解饱和氯化钠溶液:2Cl-+2H2O
H2↑+Cl2↑+2OH-,故A正确;
B.NH4HCO3溶于过量的NaOH溶液中,离子方程式为:NH4++2OH-+HCO3-═NH3.H2O+H2O+CO32-,故B错误;
C.1mol/L NaAlO2溶液和1.5mol/L的HCl溶液等体积互相均匀混合,反应的离子方程式为:6AlO2-+9H++3H2O=Al3++5Al(OH)3↓,故C错误;
D.NaClO溶液与FeCl2溶液混合,离子方程式为:3ClO2-+12Fe2++6H2O=4Fe(OH)3↓+3Cl-+8Fe3+,故D错误;
故选:A.
| ||
B.NH4HCO3溶于过量的NaOH溶液中,离子方程式为:NH4++2OH-+HCO3-═NH3.H2O+H2O+CO32-,故B错误;
C.1mol/L NaAlO2溶液和1.5mol/L的HCl溶液等体积互相均匀混合,反应的离子方程式为:6AlO2-+9H++3H2O=Al3++5Al(OH)3↓,故C错误;
D.NaClO溶液与FeCl2溶液混合,离子方程式为:3ClO2-+12Fe2++6H2O=4Fe(OH)3↓+3Cl-+8Fe3+,故D错误;
故选:A.
点评:本题考查了离子方程式的书写,题目不难,把握反应的实质是解题关键,注意反应物量的多少对反应的影响.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组离子,在指定环境中一定能大量共存的是( )
| A、在含有0.1 mol/L Ca2+的溶液中:Na+、K+、ClO-、Cl- |
| B、在pH为7的溶液中:Ag+、Mg2+、SO42-、Cl- |
| C、在澄清透明的无色溶液中:Al3+、Cu2+、HCO3-、NO3- |
| D、c(OH-)=1×10-3mol/L的溶液中:K+、SO42-、Cl-、CO32- |
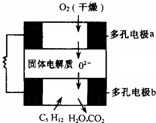 设计出燃料电池使汽油(设其成分为C5H12)氧化直接产生电流是21世纪最富有挑战性的课题之一.最近有人设计了一种固体燃料电池,固体氧化铝--氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如右图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )
设计出燃料电池使汽油(设其成分为C5H12)氧化直接产生电流是21世纪最富有挑战性的课题之一.最近有人设计了一种固体燃料电池,固体氧化铝--氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如右图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )| A、b极为电池的正极 |
| B、b极对应的电极反应式为:C5H12+16O2--32e-=5CO2+6H2O |
| C、该电池的总反应方程式为:C5H12+8O2+10OH-=5CO32-+11H2O |
| D、汽油燃料电池最大的技术障碍是氧化反应不完全,产生炭粒堵塞电极的气体通道,从而使输电效能减弱 |
1989年世界卫生组织把铝确定为食品污染源之一,而加以控制使用.铝在下列应用时应加以控制的是( )
①制铝合金 ②制电线 ③制炊具 ④银色漆颜料 ⑤明矾净水 ⑥明矾与苏打制食品膨松剂 ⑦易拉罐 ⑧用Al(OH)3凝胶制胃舒平药片 ⑨包装糖果和小食品.
①制铝合金 ②制电线 ③制炊具 ④银色漆颜料 ⑤明矾净水 ⑥明矾与苏打制食品膨松剂 ⑦易拉罐 ⑧用Al(OH)3凝胶制胃舒平药片 ⑨包装糖果和小食品.
| A、③⑤⑧⑨ | B、③⑤⑥⑦⑧⑨ |
| C、③⑤⑨ | D、⑥⑧⑨ |
下列说法中,不正确的是( )
| A、光导纤维的主要成分是SiO2 |
| B、大量排放SO2会引起酸雨 |
| C、明矾和漂白粉均可用于自来水的杀菌、消毒 |
| D、玻璃和陶瓷都属于传统硅酸盐材料 |
下列反应的离子方程式正确的是( )
| A、铁和盐酸Fe+2H+═Fe3++H2↑ |
| B、CuSO4溶液和Ba(OH)2溶液SO42-+Ba2+═BaSO4↓ |
| C、氢氧化铜和盐酸Cu(OH)2+2H+═Cu2++2H2O |
| D、铜和硝酸银溶液Cu+Ag+═Ag+Cu2+ |
 氧化还原反应在生产、生活中具有广泛用途,贯穿古今.
氧化还原反应在生产、生活中具有广泛用途,贯穿古今.