题目内容
图是某燃煤发电厂处理废气的装置示意图,下列说法不正确的是( )
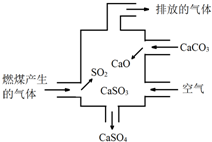

| A、使用此装置可减少导致酸雨的气体形成 |
| B、装置内发生了化合反应和分解反应 |
| C、整个过程的总反应可表示为:2SO2+2CaCO3+O2=2CaSO4+2CO2 |
| D、若排放的气体能使澄清石灰水变浑浊,说明排放的气体中含SO2 |
考点:二氧化硫的污染及治理
专题:氧族元素
分析:A.二氧化硫与氧化钙、氧气反应生成硫酸钙,可减少二氧化硫的排放,有利于减少酸雨;
B.装置内发生了碳酸钙分解生成氧化钙和二氧化碳,二氧化硫和氧化钙化合生成亚硫酸钙,亚硫酸钙与氧气发生化合反应生成硫酸钙;
C.二氧化硫与氧化钙、氧气反应生成硫酸钙,方程式为2SO2+2CaCO3+O2═2CaSO4+2CO2;
D.因为二氧化碳也能使澄清石灰水变浑浊.
B.装置内发生了碳酸钙分解生成氧化钙和二氧化碳,二氧化硫和氧化钙化合生成亚硫酸钙,亚硫酸钙与氧气发生化合反应生成硫酸钙;
C.二氧化硫与氧化钙、氧气反应生成硫酸钙,方程式为2SO2+2CaCO3+O2═2CaSO4+2CO2;
D.因为二氧化碳也能使澄清石灰水变浑浊.
解答:
解:A.二氧化硫与氧化钙、氧气反应生成硫酸钙,可减少二氧化硫的排放,有利于减少酸雨,故A正确;
B.装置内发生了碳酸钙分解生成氧化钙和二氧化碳的分解反应,二氧化硫和氧化钙化合生成亚硫酸钙和亚硫酸钙与氧气发生化合反应生成硫酸钙的化合反应,故B正确;
C.二氧化硫与氧化钙、氧气反应生成硫酸钙,方程式为2SO2+2CaCO3+O2═2CaSO4+2CO2,故C正确.
D.因为二氧化碳也能使澄清石灰水变浑浊,则排放的气体能使澄清石灰水变浑浊,不能说明排放的气体中含二氧化硫,故D错误;
故选D.
B.装置内发生了碳酸钙分解生成氧化钙和二氧化碳的分解反应,二氧化硫和氧化钙化合生成亚硫酸钙和亚硫酸钙与氧气发生化合反应生成硫酸钙的化合反应,故B正确;
C.二氧化硫与氧化钙、氧气反应生成硫酸钙,方程式为2SO2+2CaCO3+O2═2CaSO4+2CO2,故C正确.
D.因为二氧化碳也能使澄清石灰水变浑浊,则排放的气体能使澄清石灰水变浑浊,不能说明排放的气体中含二氧化硫,故D错误;
故选D.
点评:本题考查化学环境污染的治理,为高频考点,侧重化学与环境的考查,有利于培养学生良好的科学素养,提高学习的积极性,树立环保意识,难度不大.

练习册系列答案
相关题目
标准状况下,某气态烷烃和烯烃的混合气体2.24L,完全燃烧后生成4.05g水和6.6gCO2,该烃的组成为( )
| A、CH4、C3H6 |
| B、CH4、C2H4 |
| C、C2H4、C3H8 |
| D、C2H6、C3H6 |
一定条件下,下列各组物质中,Y既能与X反应又能与Z反应的是( )
| X | Y | Z | |
| ① | NaOH溶液 | Al | 稀硫酸 |
| ② | KOH溶液 | Br2 | Na2SO3溶液 |
| ③ | O2 | N2 | H2 |
| ④ | FeCl3溶液 | Cu | 浓硝酸 |
| A、只有①③④ |
| B、只有①②④ |
| C、只有①②③ |
| D、①②③④皆可 |
下列说法正确的是( )
| A、向蒸馏水中滴加浓H2SO4时,KW不变 |
| B、常温下,0.005mol?L-1Ba(OH)2溶液pH为12 |
| C、NaHCO3水解的离子方程式为:HCO3-+H2O?CO32-+H3O+ |
| D、NaHSO3属于强碱弱酸盐,其水溶液一定显碱性 |
已知0.3mol?L-1NaOH溶液的密度为ρ1 g?mL-1,0.1mol?L-11NaOH溶液的密度为ρ2 g?mL-1,若将上述两溶液等质量混合,且混合后溶液的体积等于混合前两溶液的体积之和,则所得溶液中NaOH的物质的量浓度( )
| A、大于0.2mol?L-1 |
| B、等于0.2mol?L-1 |
| C、小于0.2mol?L-1 |
| D、无法估算 |
在实验室进行下列实验,括号内的实验仪器或试剂都能用到的是( )
| A、中和热的测定(量筒、温度计、酒精灯) |
| B、从溴水中提取溴单质(分液漏斗、无水乙醇、玻璃棒) |
| C、探究浓硫酸与铜反应的产物(蘸有碳酸钠溶液的棉花团、蒸馏水、烧杯) |
| D、制氢氧化铁胶体(饱和FeCl3溶液、NaOH溶液、胶头滴管) |
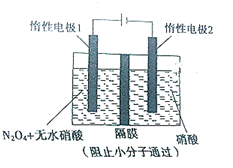 用如图装置电解制备N2O5 ,下列有关说法正确的是( )
用如图装置电解制备N2O5 ,下列有关说法正确的是( )| A、N2O5在惰性电极2处产生 |
| B、在惰性电极2处有氢气产生 |
| C、在惰性电极1处发生还原反应 |
| D、在惰性电极2处有NO产生 |
 .
.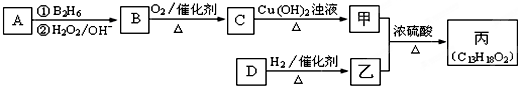
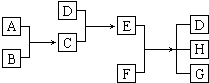 已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如图所示:
已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如图所示: