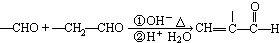题目内容
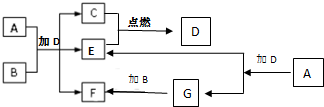 下列框图中各物质均为中学常见物质.A是淡黄色固体化合物,B、C、E为单质,其中C、E为气体,B为金属.常温、常压下D为无色液体.
下列框图中各物质均为中学常见物质.A是淡黄色固体化合物,B、C、E为单质,其中C、E为气体,B为金属.常温、常压下D为无色液体.请回答下列问题:
(1)A的化学式是
(2)B与G溶液反应的化学方程式是
(3)3.9gA与足量的D反应,转移电子的数目是
考点:无机物的推断
专题:推断题
分析:常温、常压下D为无色液体,则D是H2O,A是淡黄色固体,B是金属单质,A、B和水反应生成气体单质C、E和物质F,C、E点燃生成水,则C、E一种是氢气、一种是氧气,过氧化钠和水反应生成氧气和NaOH,则A是Na2O2,能和NaOH反应生成氢气的金属是Al,所以B是Al,过氧化钠和水反应生成氢氧化钠和氧气,所以E是O2、G是NaOH,则F是NaAlO2,据此分析解答.
解答:
解:常温、常压下D为无色液体,则D是H2O,A是淡黄色固体,B是金属单质,A、B和水反应生成气体单质C、E和物质F,C、E点燃生成水,则C、E一种是氢气、一种是氧气,过氧化钠和水反应生成氧气和NaOH,则A是Na2O2,能和NaOH反应生成氢气的金属是Al,所以B是Al,过氧化钠和水反应生成氢氧化钠和氧气,所以E是O2、G是NaOH,则F是NaAlO2,
(1)通过以上分析知,A是过氧化钠,A的化学式是Na2O2,故答案为:Na2O2;
(2)B是Al,G是NaOH,铝和氢氧化钠反应生成偏铝酸钠和氢气,反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(3)3.9gA的物质的量=
=0.05mol,过氧化钠和水反应方程式2Na2O2+2H2O=4NaOH+O2↑,该反应中有一半的过氧化钠作氧化剂、一半的过氧化钠作还原剂,所以转移电子数=0.05mol×
×2×[0-(-1)]×NA/mol=,故答案为:0.05NA.
(1)通过以上分析知,A是过氧化钠,A的化学式是Na2O2,故答案为:Na2O2;
(2)B是Al,G是NaOH,铝和氢氧化钠反应生成偏铝酸钠和氢气,反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(3)3.9gA的物质的量=
| 3.9g |
| 78g/mol |
| 1 |
| 2 |
点评:本题考查无机物推断,以物质颜色、物质状态结合转化关系采用正逆结合的方法进行推断,明确只有Al能和强碱反应是解本题关键,注意过氧化钠和水反应时既作氧化剂又作还原剂,会正确书写铝和强碱反应方程式,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
化学方程式可简明地体现元素及其化合物的性质.已知:
氧化还原反应:
FeCl3+H2S=FeCl2+S;PbO2+4HCl=PbCl2+Cl2↑+2H2O
2Fe(OH)2+Cl2+2KOH=2Fe(OH)3+2KCl;Cl2+2KOH=KCl+KClO+H2O
水溶液中的复分解反应:(Se元素的原子序数为34)
CuSO4+H2S=CuS↓+H2SO4;H2SeO4+2NaN3=Na2SeO4+2HN3;HN3+Na2S=NaN3+H2S
热分解反应:BaCO3
BaO+CO2↑;MgCO3
MgO+CO2↑;CuCO3
CuO+CO2↑
下列说法不正确的是( )
氧化还原反应:
FeCl3+H2S=FeCl2+S;PbO2+4HCl=PbCl2+Cl2↑+2H2O
2Fe(OH)2+Cl2+2KOH=2Fe(OH)3+2KCl;Cl2+2KOH=KCl+KClO+H2O
水溶液中的复分解反应:(Se元素的原子序数为34)
CuSO4+H2S=CuS↓+H2SO4;H2SeO4+2NaN3=Na2SeO4+2HN3;HN3+Na2S=NaN3+H2S
热分解反应:BaCO3
| ||
| ||
| ||
下列说法不正确的是( )
| A、氧化性(酸性溶液):PbO2>Fe3+>S |
| B、还原性(碱性溶液):Fe(OH)2>KCl>Cl2 |
| C、酸性(水溶液):H2S>H2SO4>H2SeO4>HN3 |
| D、热稳定性:BaCO3>MgCO3>CuCO3 |
在溶液中加入足量Na2O2后仍能大量共存的离子组是( )
| A、Mg2+、Ba2+、Cl-、NO3- |
| B、K+、AlO2-、Cl-、SO42- |
| C、Na+、K+、NO3-、HCO3- |
| D、Al3+、Cl-、CO32-、K+ |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、遇苯酚变紫色的溶液:Na+、Mg2+、SO42-、Cl- |
| B、0.1 mol?L-1 (NH4)2Fe(SO4)2溶液中:K+、Cu2+、Cl-、MnO4- |
| C、使甲基橙变红色的溶液:NH4+、Cu2+、ClO-、Cl- |
| D、0.1mol?L-1 NaHCO3溶液:K+、AlO2-、Cl-、NO3- |